题目内容
亚硫酸钠(Na2SO3)中硫元素的化合价为
- A.-2
- B.+2
- C.+4
- D.+6
C
分析:根据在化合物中正负化合价代数和为零,结合亚硫酸钠(Na2SO3)的化学式进行解答本题.
解答:钠元素显+1,氧元素显-2,设硫元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)×2+x+(-2)×3=0,则x=+4.
故选C.
点评:本题难度不大,考查学生利用化合价的原则计算指定元素的化合价的能力.
分析:根据在化合物中正负化合价代数和为零,结合亚硫酸钠(Na2SO3)的化学式进行解答本题.
解答:钠元素显+1,氧元素显-2,设硫元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)×2+x+(-2)×3=0,则x=+4.
故选C.
点评:本题难度不大,考查学生利用化合价的原则计算指定元素的化合价的能力.

练习册系列答案
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案 应用题作业本系列答案
应用题作业本系列答案
相关题目
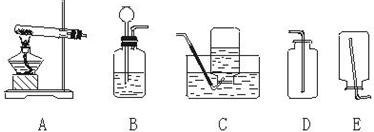
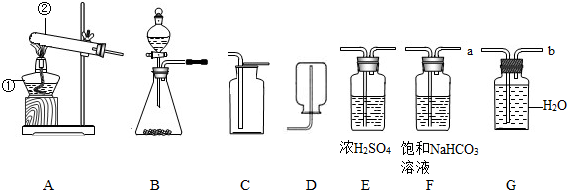
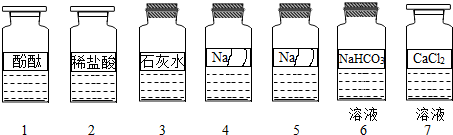
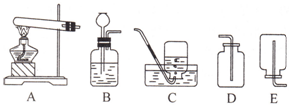 实验室常亚亚硫酸钠(Na2SO3)固体与稀硫酸在常温下反应制取二氧化硫气体,且同时生成硫酸钠和水.已知二氧化硫的密度比空气的大,溶于水且与水反应生成亚硫酸(H2SO3).
实验室常亚亚硫酸钠(Na2SO3)固体与稀硫酸在常温下反应制取二氧化硫气体,且同时生成硫酸钠和水.已知二氧化硫的密度比空气的大,溶于水且与水反应生成亚硫酸(H2SO3).