题目内容
氧化铜和铜的混合物2g,用氢气完全还原后得到铜粉的质量为1.8g,求:
(1)原混合物中氧化铜的质量是多少.
(2)原混合物中铜元素的质量分数是多少?
(1)原混合物中氧化铜的质量是多少.
(2)原混合物中铜元素的质量分数是多少?
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:根据完全还原后得到铜粉的质量可以计算氧化铜的质量,进一步可以计算原混合物中氧化铜的质量和原混合物中铜元素的质量分数.
解答:解:设氧化铜的质量为x,
CuO+H2
Cu+H2O,固体质量差
80 64 16
x 2g-1.8g
=
,
x=1g,
答:原混合物中氧化铜的质量是1g.
(2)原混合物中铜元素的质量分数为:
×100%=90%,
答:原混合物中铜元素的质量分数为90%.
CuO+H2
| ||
80 64 16
x 2g-1.8g
| 80 |
| 16 |
| x |
| 2g-1.8g |
x=1g,
答:原混合物中氧化铜的质量是1g.
(2)原混合物中铜元素的质量分数为:
| 1.8g |
| 2g |
答:原混合物中铜元素的质量分数为90%.
点评:本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
包装食品时,能用作保护气的一组气体是( )
| A、H2、N2 |
| B、N2、O2 |
| C、CO2、H2 |
| D、N2、CO2 |
关于Mg和Mg2+两种微粒叙述正确的是( )
| A、质子数相同 |
| B、电子层数相同 |
| C、最外层电子数相同 |
| D、化学性质相同 |
 在研究二氧化碳的性质时,老师做了如图1所示实验,该实验说明二氧化碳具有
在研究二氧化碳的性质时,老师做了如图1所示实验,该实验说明二氧化碳具有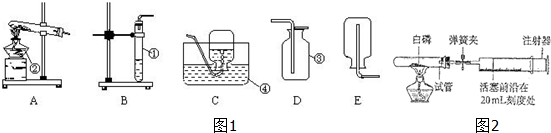
 过滤是一种净水的方法,可以用来分离不溶性固体和液体.
过滤是一种净水的方法,可以用来分离不溶性固体和液体.