题目内容
【题目】实验室有一瓶长期存放的固体氢氧化钠,由于保管不当已经变质。某兴趣小组的同学欲通过实验测定其变质的情况,实验过程如下:取样品25g放入烧杯中,向其中加入280g过量的稀盐酸,得到296.2g溶液。试计算:
(1)产生的气体的质量为__________;
(2)25g样品中氢氧化钠的质量_________。
【答案】8.8g 3.8g
【解析】
根据质量守恒定律,反应前后减少的质量就是生成二氧化碳的质量,根据二氧化碳质量计算碳酸钠质量,最后计算氢氧化钠质量。
(1)二氧化碳质量为25g+280g-296.2g=8.8g。
(2)设样品中碳酸钠的质量为x。
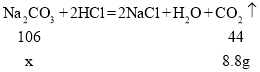
![]() ,x=21.2g,
,x=21.2g,
样品中氢氧化钠的质量=25g-21.2g=3.8g
答:产生气体8.8g;样品中氢氧化钠的质量为3.8g。

 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案【题目】某兴趣小组活动中,同学们按图1装置对“可燃物燃烧的条件”进行探究,探究过程中,大家对磷燃烧生成的大量白烟是否危害人体健康提出疑问。
(查阅资料)白磷的着火点是40℃,红磷的着火点是240℃,燃烧产物五氧化二磷是白色固体,会刺激人体呼吸道,并能与空气中的水蒸气反应,生成有毒的偏磷酸(H2PO3)。
(交流与讨论)白烟对人体健康有害,该实验装置必须改进。
(改进与实验)同学们按改进后的图2装置进行实验。

请你帮助他们将下表补充完整。
实验现象 | 对实验现象的解释 |
a试管中白磷燃烧,热 水中白磷没有燃烧 b试管中红磷没有燃烧 | (1)热水中白磷没有燃烧的原因是___________ (2)b试管中红磷没有燃烧的原因是________ |
(反思与评价)
(3)改进后的图2装置与图1装置比较的优点是___________。
(4)小雅同学指出图2装置仍有不足之处,并设计了图3装置,其中气球的作用是___________。
(5)检查完装置的气密性之后,小实进行了上述实验。实验小结时,小实同学认为还可以用冷却后的a试管测定空气中氧气的含量,他的操作是___________最终发现进入a试管内液体的体积小于试管容积的![]() ,如果不考虑橡皮塞占试管的容积,出现这种现象的原因可能是________。
,如果不考虑橡皮塞占试管的容积,出现这种现象的原因可能是________。