题目内容
【题目】通过晾晒海水或者煮盐井水、盐湖水等,可以蒸发除去水分,得到粗盐。粗盐中含有多种可溶性杂质(氯化镁、氯化钙等)和不溶性杂质(泥沙等)。工业上以粗盐为原料制取精盐,其生产流程如图所示:
请回答下列问题:
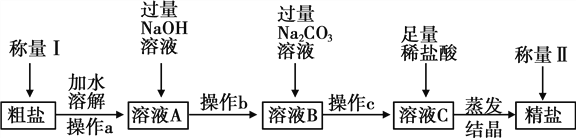
(1)已知操作a、b、c中均含同一种操作,其名称是_________。
(2)将足量稀盐酸加入溶液C中,反应的化学方程式为(任写一个)____________________。
(3)在蒸发操作中,用玻璃棒搅拌的作用是________________________。
(4)如果称量Ⅰ中称得粗盐的质量为5 g,称量Ⅱ中称得精盐的质量为5.1 g,则下列分析正确的是____。
A.精盐的产率一定为98.04% B.精盐的产率一定为102%
C.蒸发操作中可能有水分没有蒸干 D.溶解操作中可能有粗盐没有溶解
E.除杂过程中有NaCl生成
【答案】(1)过滤
(2)NaOH+HCl=NaCl+H2O
(3)使液体受热均匀,防止局部过热造成液滴飞溅
(4)CE
【解析】试题分析:
(1)过滤可以将不溶性固体从溶液中分离出来,所以操作a、b、c中均含同一种操作,其名称是过滤;
(2)氢氧化钠和盐酸反应生成氯化钠和水,化学方程式为:NaOH+HCl=NaCl+H2O;
(3)在蒸发操作中,用玻璃棒搅拌的作用是使液体受热均匀,防止局部过热造成液滴飞溅;
(4)计算粗盐提纯的产率时,粗盐必须全部溶解,氢氧化钠、碳酸钠在除杂的过程中会生成氯化钠,所以A.精盐的产率可能为98.04%,故错误;B.精盐的产率可能为102%,故B错误;C、蒸发操作中可能有水分没有蒸干,可能导致产率偏大,故正确;D.溶解操作中粗盐必须全部溶解,故错误;E.除杂过程中有NaCl生成,故E正确。故选:CE。

练习册系列答案
 新思维寒假作业系列答案
新思维寒假作业系列答案
相关题目