题目内容
【题目】二氧化氯(ClO2)是一种高效,安全的消毒剂。
(1)工业上生产NaClO2的化学方程式为: 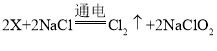 ,则X的化学式为______;反应前后化合价发生改变的元素是_____。
,则X的化学式为______;反应前后化合价发生改变的元素是_____。
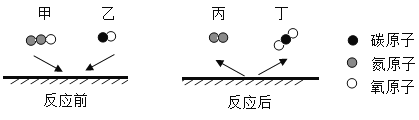
(2)在一定条件下,C1O2气体与氰化氢(HCN)反应(未配平)的微观示意图如图。
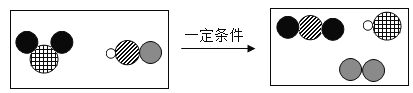
写出上图表示的化学方程式为_____,反应生成的N2与CO2的质量比为____。
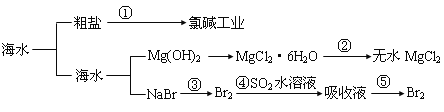
(3)某同学在学习中构建了“氯及其化合物的价、类关系图”
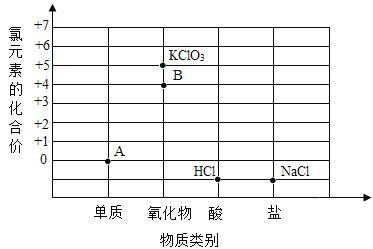
①已知由氯元素组成的单质是双原子分子,写出图中A点对应物质的化学式____。
②与图中的点对应物质类别不相符合的化学式所表示的物质名称是_______。
③HCl气体是由_____。(填“分子”、“原子”或“离子”)构成的。
【答案】ClO2 Cl 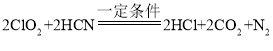 7:22 Cl2 氯酸钠 分子
7:22 Cl2 氯酸钠 分子
【解析】
(1)根据质量守恒定律,化学反应前后,原子的种类和数目不变,结合化学方程式: ,反应物中含2个钠原子、2个氯原子,生成物中含2个钠原子、4个氧原子、4个氯原子,故反应物中还应含4个氧原子、2个氯原子,故X的化学式为:ClO2;
,反应物中含2个钠原子、2个氯原子,生成物中含2个钠原子、4个氧原子、4个氯原子,故反应物中还应含4个氧原子、2个氯原子,故X的化学式为:ClO2;
氧元素通常为-2价,设ClO2中氯元素的化合价为x,根据化合物中,正、负化合价的代数和为零,可得:x+(-2)×2=0,x=+4;
氯化钠中钠元素为+1价,氯元素为-1价;
氯气中氯元素为0价;
NaClO2中钠元素为+1价,氧元素为-2价,设氯元素的化合价为y,根据化合物中,正、负化合价的代数和为零,可得:(+1)+y+(-2)×2=0,y=+3
故反应前后化合价发生改变的元素是Cl;
(2)由图可知,该反应为ClO2气体与氰化氢(HCN)在一定条件下反应生成二氧化碳、氯化氢和氮气,该反应的化学方程式为: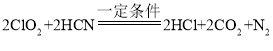 ;
;
根据化学方程式,反应生成的N2与CO2的质量比为:(14×2):(2×44)=7:22;
(3)①图中A点对应的物质为单质,且氯元素的化合价为0,故是氯元素组成的单质,已知氯元素组成的单质是双原子分子,故该物质的化学式为:Cl2;
②NaClO3由钠、氯、氧三种元素组成,故不属于氧化物,与与图中的点对应物质类别不相符合,该物质的名称是:氯酸钠;
③HCl气体是由氯化氢分子构成的,故填:分子。

 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案 海淀课时新作业金榜卷系列答案
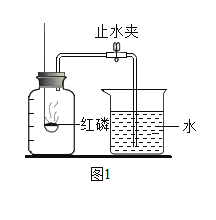
海淀课时新作业金榜卷系列答案【题目】某兴趣小组的同学按照课本单元练习上的实验装置做“测定空气中氧气的体积分数”实验(如图1所示),但测出的氧气的体积分数明显小于理论值。请参与探究:
(1)提出问题:造成误差的原因是什么?如何改进课本上的实验装置?
(2)查阅资料:红磷、白磷的一些性质如下表:
颜色、状态 | 熔点/℃ | 着火点/℃ | 密度/(g/cm3) | |
红磷 | 暗红色固体 | 590 | 240 | 2.34 |
白磷 | 白色或黄色固体 | 44.1 | 40 | 1.82 |
(3)猜想与假设:
①可能是导管内原来含有空气,后来又残留有吸入的水。
②你还能作出的猜想是_____、____。
(4)交流与讨论:
某同学认为可用木炭代替红磷来消除误差,他的猜想不合理的原因是______。
(5)探究与反思:
将铜粉放在残余气体中加热,观察到铜粉变黑色,说明__________。
(6)改进实验:
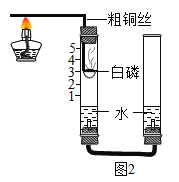
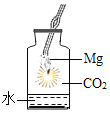
①他们对课本上的实验装置进行了图2所示的改进(其他图2仪器忽略),把红磷换为白磷理由是________。
②大家用改进的实验装置(如图2所示)进行实验,待玻璃管冷却、管内白烟消失时,左玻璃管内的液面上升了___格,得到了较准确的结果。
【题目】化学实践活动课上,老师拿来一包粉末。它是由长期放置在空气中的铁粉和久置的碱石灰干燥剂混合而成。让同学们设计实验进行探究。
[提出问题]固体样品的成分是什么?
[查阆资料] (1)碱石灰干燥剂是CaO和NaOH的混合物。
(2)BaCl2溶液是中性。
[猜想与假设]
固体样品中可能含有Fe、Fe2O3、 CaO、 NaOH、Ca(OH)2、Na2CO3和_________等七种物质。
[进行实验]如图
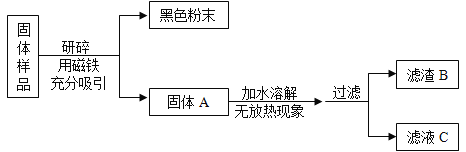
甲组同学对滤渣B的成分进行探究,记录如下:
实验操作 | 实验现象 | 实验结论及化学方程式 |
取少量滤渣B于试管中,加入足量稀盐酸,将生成的气体通入澄清的石灰水中 | ①____ ②_____ | 结论:滤渣B中有Fe2O3、CaCO3。实验操作中反应的化学方程式为:__ |
乙组同学对滤液C的成分进行了探究。记录如下:
实验操作 | 实验现象 | 实验结论 |
取少量滤液C于试管中,加入过量BaCl2溶液,静置,向上层清液中滴加无色酚酞试液,振荡 | ①有白色沉淀生成 ②酚酞试液由无色变成红色 | 滤液C中有___ |
[解释与结论]
(1)乙组同学实验中加入过量BaCl2溶液的目的是__________。
(2)通过以上实验探究。该固体样品中能确定一定含有的成分是_______。