题目内容
【题目】学习了二氧化锰对过氧化氢分解有催化作用的知识后,某同学想:氧化铜能否达到类似二氧化锰的催化作用呢?于是进行了以下探究。
(猜想)氧化铜能作过氧化氢分解的催化剂。
(实验)用天平称量0.4g氧化铜,取5mL5%的过氧化氢溶液于试管中,进行如下实验。
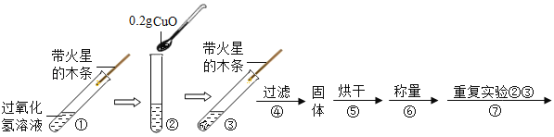
(1)填写下表:
步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
_______,带火星的木条复燃 | 0.4g氧化铜 | 溶液中有气泡放出,_________ | 猜想成立 |
(2)步骤①的目的是_________。
(3)过氧化氢被氧化铜催化分解放出氧气的文字表达式_________。
(4)步骤⑦是为了探究_________。
【答案】有气泡产生 带火星的木条复燃 进行对比 过氧化氢![]() 水+氧气 氧化铜的化学性质在反应前后没有发生改变
水+氧气 氧化铜的化学性质在反应前后没有发生改变
【解析】
解:(1)氧化铜对过氧化氢的分解有催化作用,能加快其分解速率生成氧气的速率,故步骤③中的现象是有气泡产生,带火星的木条复燃;催化剂的特点是“一变,两不变”,反应前后其质量不变,所以步骤⑥中称量的氧化铜的质量仍为0.4g;催化剂的特点是“一变,两不变”,其中反应速率改变,这里是加快,反应后化学性质不变,故氧化铜依然起到催化作用,所以⑦的现象是溶液中有气泡放出,带火星的木条复燃;
(2)为了看氧化铜是否能改变反应的速率,要通过加入氧化铜与不加氧化铜的现象进行对比,才能得出科学合理的结论;
(3)过氧化氢在氧化铜的催化作用下分解生成水和氧气,文字表达式为:过氧化氢![]() 水+氧气;
水+氧气;
(4)步骤⑦的目的是证明氧化铜的化学性质在反应前后没有发生改变。

【题目】如图所示,市场上销售的一种真空充气包装的形如小枕头的“蛋黄派”, 它“鼓鼓”的包装和松软的口感受到人们的关注。请用所学知识探究以下问题:

(1)“鼓鼓”的袋内所充气体的作用是________。
(2)小明同学认为袋内无色无味的气体是氮气,并用燃着的木条检验他的猜想.请你评价该检验方法的可行性:_________________(简述理由)。
(3)小红同学猜想是二氧化碳。请你帮助她设计一个简单的实验方案,用以验证其猜想是否正确:
实验步骤 | 现象和结论 |
________________ | ________________________ |
(4)你认为食品充气包装,对所充气体的要求是:
①____________; ②_________; ③_________。