题目内容
兴趣小组的同学为了探究木炭在高温条件下还原氧化铜所生成的气体产物是什么,提出了猜想:
a.气体产物可能是二氧化碳;
b.气体产物可能是一氧化碳;
c.气体产物可能是二氧化碳和一氧化碳的混合物.
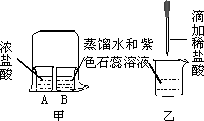
(1)同学们设计了如图所示装置(铁架台已略去),通过实验探究气体产物的成分.

已知NaOH溶液能够快速吸收二氧化碳,则装置C的作用是________.
实验过程中观察到A、E装置中的澄清石灰水均变浑浊,C装置中的澄清石灰水不变浑浊,由此可得出该气体产物的成分为________.装置A、E中发生反应的化学方程式为________.
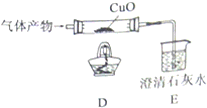
(2)有同学提出,从简约装置、节约实验药品的角度出发,上图装置可进行改进,去掉A、B、C装置,只用D、E装置同样可以探究出该气体产物的成分(如图所示).请你写出其实验操作过程(写出操作步骤,不需要写出现象和结论):
________.
解:(1)从气体依次通过澄清石灰水→氢氧化钠溶液→澄清石灰水→氧化铜→澄清的石灰水,可以分析气体第一次通过澄清石灰水是为了检验气体中有没有二氧化碳,然后通过氢氧化钠是吸收二氧化碳因为氢氧化钙在水中的溶解度小应选用氢氧化钠吸收大量的二氧化碳,再通过澄清的石灰水是为了检验二氧化碳是否除净,然后一氧化碳通入氧化铜加热和氧化铜反应生成铜和二氧化碳,最后将从氧化铜中出来的气体再通入澄清石灰水中若变浑浊则说明原气体中含有一氧化碳.若A、E装置中的澄清石灰水均变浑浊,C装置中的澄清石灰水不变浑浊,由此可得出该气体产物的成分为一氧化碳和二氧化碳的混合物.
故(1)答案:检验二氧化碳是否已除尽 一氧化碳和二氧化碳的混合物 CO2+Ca(OH)2=CaCO3↓+H2O
(2)D先不加热将气体通入E,若E中的澄清石灰水变浑浊说明气体中含有二氧化碳,再加热D观察D中的黑色固体是否变红色因为一氧化碳和氧化铜反应生成红色的铜和二氧化碳即可确定气体的成分.故(2)答案:先通气体观察E中的现象,然后再加热观察D中的现象
分析:(1)运用二氧化碳能使澄清的石灰水变浑浊的性质、A、E中的石灰水都变浑浊和一氧化碳能在加热的条件下和氧化铜反应生成铜和二氧化碳的性质,然后分析图中装置的操作目的解答.
(2)运用一氧化碳与氧化铜反应生成铜和二氧化碳、一氧化碳不能使澄清的石灰水变浑浊但二氧化碳能使澄清的石灰水变浑浊解答.
点评:本题从木炭还原氧化铜、二氧化碳气体的检验和除去方法设置考点,体现了化学的实验学科的特点,这就要求同学们不断培养运用所学知识进行探究实验的能力和意识.
故(1)答案:检验二氧化碳是否已除尽 一氧化碳和二氧化碳的混合物 CO2+Ca(OH)2=CaCO3↓+H2O
(2)D先不加热将气体通入E,若E中的澄清石灰水变浑浊说明气体中含有二氧化碳,再加热D观察D中的黑色固体是否变红色因为一氧化碳和氧化铜反应生成红色的铜和二氧化碳即可确定气体的成分.故(2)答案:先通气体观察E中的现象,然后再加热观察D中的现象
分析:(1)运用二氧化碳能使澄清的石灰水变浑浊的性质、A、E中的石灰水都变浑浊和一氧化碳能在加热的条件下和氧化铜反应生成铜和二氧化碳的性质,然后分析图中装置的操作目的解答.
(2)运用一氧化碳与氧化铜反应生成铜和二氧化碳、一氧化碳不能使澄清的石灰水变浑浊但二氧化碳能使澄清的石灰水变浑浊解答.
点评:本题从木炭还原氧化铜、二氧化碳气体的检验和除去方法设置考点,体现了化学的实验学科的特点,这就要求同学们不断培养运用所学知识进行探究实验的能力和意识.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目