题目内容
(4分)人类生产生活离不开钢铁。生铁和钢都是铁的合金。某同学将10 g铁的合金样品投入足量稀硫酸中,充分反应(合金中除铁外其他成分不与稀硫酸反应)。测得产生气体的质量为0.35 g。计算该合金中铁的质量分数。
解:设样品合金中铁的质量为m。
根据Fe+H2SO4===FeSO4+H2↑(1分)
56 2
m 0.35 g(1分)
则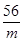 =
=
解得m=9.8 g(1分)
所以合金中铁的质量分数为 ×100%=98%。(1分)
×100%=98%。(1分)
答:该合金中铁的质量分数为98%。
解析

练习册系列答案
相关题目
(4分)人类生活和工农业生产都离不开水,下图是自来水厂净化水的过程示意图:
请根据图示回答下列问题:
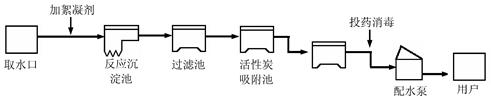
(1)自来水厂生产自来水时,使用的净水方法有___________(填序号)。
| A.沉淀 | B.过滤 | C.煮沸 | D.蒸馏 E.吸附 |
(3)自来水厂用ClO2消毒,漂白粉2可用于饮用水消毒。工业上制备漂白粉的化学方程式为:2Cl2+2Ca(OH)2=X+Ca(ClO)2+2H2O, X的化学式为 。
(4)节约用水人人有责,请举出一种节水的措施________________________________。