题目内容
我国拥有自主知识产权的硅衬底高光效氮化镓发光二极管(简称LED)技术,已广泛用于照明、显像等多个领域。氮和镓的原子结构示意图及镓在元素周期表中的信息如下图所示,下列说法正确的是( )
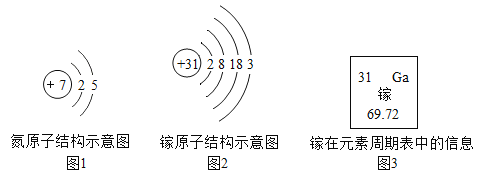
A.镓元素位于第三周期,属于金属元素 B.镓原子核内有31个中子
C.镓的相对原子质量是69.72g D.氮化镓的化学式为GaN
我国自主设计的大型客机成功试飞,国产航母下水,标志着我国的金属材料制造技术取得重大突破。根据所学知识回答下列问题:
金属 | A | B | C | D |
导电性(以100为标准) | 99 | 61 | 17 | 7.9 |
密度/(g﹒cm-3) | 8.92 | 2.70 | 7.86 | 11.3 |
熔点/°C | 1083 | 660 | 1535 | 327 |
硬度(以10为标准) | 3 | 2.7 | 5 | 1.5 |
(1)常温下一些金属的物理性质数据如表,据此可知高压输电线最好选用金属_____(填字母);C的合金通常可以做菜刀、锤子等,其合金的硬度_____5(填“>”“<”或“=”)。
(2)铁矿石有多种,如赤铁矿(主要成分Fe2O3)和磁铁矿(主要成分Fe3O4)等,写出磁铁矿的主要成分与一氧化碳反应的化学方程式_____。
(3)某兴趣小组为探究Zn、Fe、Cu、Ag四种金属的活动性,进行如下图中甲、乙、丙三个实验。
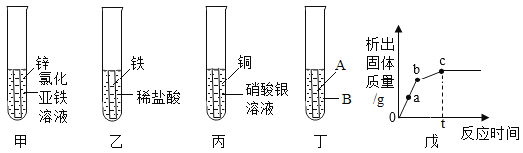
①小组同学随后发现该实验无法得出四种金属的活动性顺序。于是补充图丁实验,最终得出四种金属活动性:Zn>Fe>Cu>Ag,则图丁中的试剂A、B分别为_____(写出一组即可)。
③小组同学将丙试管中的物质过滤后、向滤液中加入甲中剩余的锌,析出固体质量的变化随反应时间的关系如戊图所示。写出a点对应溶液中所含的溶质是_____(填化学式)。
某化学兴趣小组的同学,通过咨询老师准备用亚硫酸钠溶液与浓硫酸反应来制备一定量的 ]。老师给他们提供了一瓶亚硫酸钠溶液并告知该瓶溶液放置时间可能较长,不知是否变质。兴趣小组的同学分成甲、乙两小组对该瓶亚硫酸钠溶液成分进行实验探究。
]。老师给他们提供了一瓶亚硫酸钠溶液并告知该瓶溶液放置时间可能较长,不知是否变质。兴趣小组的同学分成甲、乙两小组对该瓶亚硫酸钠溶液成分进行实验探究。
[提出问题]该瓶溶液中溶质的成分是什么?该瓶溶液中亚硫酸钠的质量分数是多少?
[查阅资料]
a、Na2SO3有较强还原性,在空气中易被氧气氧化: ;
;
b、Na2SO3能与酸反应产生SO2气体;
c、SO32-、SO42-均能与Ba2+反应产生白色沉淀,BaSO3可溶于稀盐酸。
[作出猜想]
猜想1:没有变质,成分是Na2SO3;
猜想2:完全变质,成分是Na2SO4;
猜想3:部分变质,成分是Na2SO3和Na2SO4。
[实验探究I]甲组设计实验探究溶液是否变质:
甲组 | 实验操作 | 现象 | 结论 |
步骤1 | 取少量样品于试管中加入过量稀盐酸。 | 产生气泡 | 溶液中含有_____ |
步骤2 | _____ | _____ | 溶液中含有Na2SO4 |
实验结论是_____。
[实验探究Ⅱ]乙组设计如下实验测定Na2SO3溶液的溶质质量分数。

(1)连好装置并检查装置气密性,在锥形瓶中放人126g该样品,通入N2的目的是_____。
(2)实验前称量C装置的质量为128.8g。
(3)关闭活塞K,用注射器推入浓硫酸至不再产生气泡,注射器可以换为_____,也能控制液体试剂的滴加速率。
(4)打开活塞K,缓缓鼓入一定量的N2,继续通入N2的作用是_____。
(5)再次称量C装置的质量为135.2g。
(6)计算出该溶液中Na2SO3的质量分数为10%,若没有D装置,实验结果将_____(填“偏大”“不变”或“偏小”)。
[反思]由此可得出,保存亚硫酸钠时应_____。


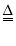 MnCl2+Cl2↑+2H2O ②3Cl2+2Fe(OH)3+xKOH=2K2FeO4+6KCl+yH2O下列说法正确的是
MnCl2+Cl2↑+2H2O ②3Cl2+2Fe(OH)3+xKOH=2K2FeO4+6KCl+yH2O下列说法正确的是