题目内容
科学家发明了一种在厌氧微生物作用下处理水中有机物(以C6H1005为例)的新技术,其原理可表示为:2C6H1005+202═7C02+5x,则x的化学式是( )
| A、CH4 | B、CH40 | C、C2H4 | D、H20 |
练习册系列答案
相关题目
氯化钠是一种重要的化工原料.电解氯化钠溶液可制得氢氧化钠等物质,反应的化学方程式为2NaCl+2H2O
X↑+H2↑+2NaOH.则X的化学式为( )
| ||
| A、Cl2 |
| B、HCl |
| C、HClO |
| D、HClO3 |
下列4个图象能正确反映对应变化关系是( )
| A | B | C | D |
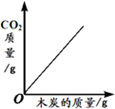 |  | 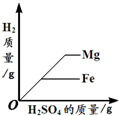 | 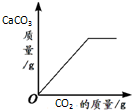 |
| 引燃密闭集气瓶中的木炭(过量) | 向盛有一定量碳酸钙粉末的烧杯中加入稀盐酸 | 向等质量的镁、铁两种金属中分别加入同浓度的足量稀硫酸 | 向盛有一定量的Ca(OH)2溶液的烧杯中通入CO2 |
| A、A | B、B | C、C | D、D |
下列图象能正确反映对应变化关系的是( )
A、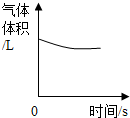 红磷在密闭的空气中燃烧 | B、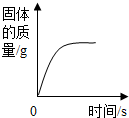 镁带在充足的氧气中燃烧 | C、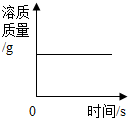 一定量的稀硫酸中加入锌粒 | D、 向某温度时的饱和食盐水中加入食盐 |
下列有关对质量守恒定律的理解,正确的是( )
| A、5g硫和5g氧气完全反应后,生成物的质量为10g | B、化学反应前后分子的总数一定不会发生变化 | C、镁条燃烧后质量增加,不遵循质量守恒定律 | D、将5g铁和5g铜混合加热后,物质的总质量为10g,遵循质量守恒定律 |
3.0g某物质完全燃烧后只生成4.4g CO2和1.8g水,下列判断正确的是( )
| A、该物质由碳、氢、氧元素组成 | B、该物质只含碳、氢元素 | C、该物质一定含有碳、氢元素,可能含有氧元素 | D、该物质的分子中碳原子和氢原子的个数比为1:2 |
科学研究表明,氨气在常压下就可以液化为液氨.液氨具有可燃性,可用作汽车的清洁燃料.氨气在一定条件下可以与氧气发生如下反应:4NH3+5O2
4X+6H2O.下列说法中不正确的是( )
| ||
| A、氨气在常压下液化是物理变化 |
| B、氨气和液氨都属于单质 |
| C、液氨具有可燃性属于化学性质 |
| D、X的化学式为NO |
下列应用的原理(用化学方程式表示)及基本反应类型均正确的是( )
A、用赤铁矿高炉炼铁 Fe2O3+3CO
| ||||
| B、硫酸厂污水可用熟石灰中和处理 H2SO4+Ca(OH)2═CaSO4+H2O 复分解反应 | ||||
C、加热混有二氧化锰的氯酸钾制取氧气 2KClO3
| ||||
D、用红磷测定空气中氧气含量 4P+5O2
|
下列化学方程式符合题意且书写正确的是( )
A、用点燃的方法出去二氧化碳中少量的一氧化碳:2CO+O2
| ||||
| B、正常雨水的pH约为5.6的原因:CO2+H2O═H2CO3 | ||||
| C、工业上用熟石灰和纯碱制取烧碱:Na2CO3+Ca(OH)2═CaCO3↓+NaOH | ||||
| D、实验室中敞口放置的氢氧化钠固体部分变质:2NaOH+CO2═NaCO3+H2O |
