题目内容
【题目】甲、乙、丙三位同学对氯化镁样品(仅含氯化铝杂质)进行如下检测:取457g样品溶于一定量的水中得到8000g溶液,再逐渐加入固体氢氧化钠,反应得到沉淀和加入的氢氧化钠的质量图象如图:(已知氢氧化铝沉淀可以和氢氧化钠溶液反应生成无色溶液,反应方程式为Al(OH)3+NaOH═NaAlO2+2H2O)
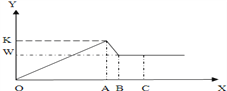
X轴表示加入氢氧化钠的质量,Y轴表示生成沉淀的质量.W为116克,K为272克,试回答下列问题:
(1)如图图象中,A点氢氧化钠的质量为 g,B点氢氧化钠的质量与A点氢氧化钠的质量的差值为 g.
(2)计算氯化镁样品的质量分数(保留到0.01),写出过程.
【答案】(1)400;80.
(2)41.58%
【解析】(1)设氯化镁质量为x,和氯化镁反应的氢氧化钠质量为y,和氯化铝反应的氢氧化钠质量为z,
氢氧化铝沉淀可以和氢氧化 钠溶液反应生成无色溶液,而氢氧化镁不与氢氧化钠溶液反应,所以反应生成氢氧化铝质量为:272g﹣116g=156g,
MgCl2+2NaOH═Mg(OH)2↓+2NaCl,AlCl3+3NaOH═Al(OH)3↓+3NaCl,
95 80 58 120 78
x y 116g z 156g
95/x=80/y=58/116g, 120/z=78/156g
x=190g,y=160g,z=240g,
如图图象中,A点氢氧化钠的质量为:160g+240g=400g;
设溶解156g氢氧化铝需要氢氧化钠的质量为m,
Al(OH)3+NaOH═NaAlO2+2H2O,
78 40
156g m
78/156g=40/m
m=80g,
因此B点 氢氧化钠的质量与A点氢氧化钠的质量的差值为80g.
故填:400;80.
(2)样品中氯化镁的质量分数为:190g÷457g×100%=41.58%,
答:样品中氯化镁的质量分数为41.58%

【题目】对比分析不同物质的共性与差异性是学习化学有效方法。下列关于CO2和CO的各项对比,有错误的是
选项 | 共性 | 差异性 |
A | 均由分子构成 | 分子的结构不同 |
B | 均由碳元素和氧元素组成 | 元素的质量比不同 |
C | 常温下均是无色气体 | 相同条件下气体的密度不同 |
D | 均能与水化合 | 化合现象不同 |
A. A B. B C. C D. D

