题目内容
【题目】化学与生活息息相关。请回答下列问题:
(1)净化水的操作有过滤、蒸馏、静置沉淀等多种,其中净化程度最高的操作是________。新装修的房子中经常放入一些活性炭包,主要利用活性炭的______作用。
(2)生活中常用铁锅做饭,主要利用了铁的_______性。在厨房炒菜时,在客厅都能闻到菜香味的主要原因是________。
(3)使用碳素墨水书写的文字很长时间不变色,是因为__________。
(4)油炸食物不宜多吃,因为长时间煎炸会产生有毒物质丙烯醛,该物质在空气中可以完全燃烧,其燃烧的化学方程式可表示为: ,则X的化学式为________。
,则X的化学式为________。
【答案】蒸馏 吸附 导热 分子在不断的运动 常温下,碳化学性质稳定 C3H4O
【解析】
(1)通过蒸馏除去了水中所有的杂质,所得到的水为纯净物,净化程度最高;活性炭具有疏松多孔结构,具有吸附性;
(2)铁锅常用于做饭,是利用了铁的导热性;闻到菜香味的主要原因是分子在不断的运动;
(3)常温下,碳化学性质稳定,所以使用碳素墨水书写的文字很长时间不变色;
(4)反应后总共有6C、8H、16O,反应前有14O,故X中含有3C、4H、1O,化学式为:C3H4O。

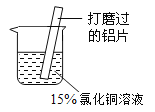
【题目】某化学兴趣小组同学在实验室研究铝与氯化铜溶液的反应,进行了如下探究:
实验操作 | 实验现象 |
| ①有红色物质附着于铝片表面 ②铝片表面逸出大量无色气体,放出大量的热 ③烧杯底部出现红色沉淀和白色沉淀 |
(1)打磨铝片的目的是_________________。
(2)现象①和现象③中的红色物质均为Cu,生成该物质的化学方程式为____________。
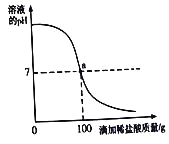
(3)经检验,现象②中的无色气体为氢气。甲同学猜测可能是氯化铜溶液显酸性,经pH计检验,pH<7,证实了甲的猜想。
(查阅资料)
①氯化亚铜(CuCl)可与浓氨水反应生成无色的Cu(NH3)2+和Cl-。
②Cu(NH3)2+,在空气中易被氧化变为蓝色;Cl-可与硝酸银溶液反应,产生白色沉淀。
(4)探究白色沉淀的化学成分:
乙同学通过查阅资料认为白色沉淀可能是CuCl。
已知CuCl是一种微溶于水的白色固体,在空气中易被氧化成唯一褐色产物Cu(OH)Cl,该反应的化学方程式为__________。
(进行实验)
①取烧杯底部的白色沉淀,充分洗涤;
②向其中加入浓氨水,沉淀溶解得到无色溶液,将无色溶液分为两份;
③取其中一份无色溶液……
④将另一份无色溶液放置于空气中…
以上步骤③的实验方案是___________;步骤④的现象是___________。
(得出结论)通过实验可以确定,该白色固体是CuCl。
(反思与评价)Al和CuCl2溶液反应为什么会出现CuCl呢?
丙同学猜测:可能是Cu与CuCl2溶液反应生成了CuCl。
丙同学为了验证猜想,取Cu粉与15%CuCl2溶液混合,无白色沉淀产生。
(5)丙通过分析Al与CuCl2溶液反应的实验现象,改进了实验,证明了Cu与CuCl2溶液反应生成了CuCl2,改进之处是____________。
(6)丁同学认为丙同学的实验还不够严谨,还应考虑________对Cu与CuCl2溶液反应的影响。
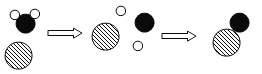
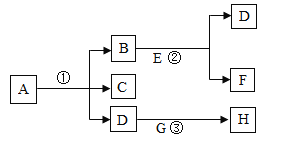
【题目】为提高煤的利用率,可将碳与水蒸气在高温的条件下反应得到两种可燃性气体,其微观示意图如下
化学变化的微观示意图 | 说明 |
|
|
(1)根据质量守恒定律判断,上述微观示意图中缺少的微粒是___________。
A ![]() B
B ![]() C
C ![]() D
D ![]()
(2)写出该反应的化学方程式___________________________,氧化剂是___________。
(3)经研究发现氨气燃烧的产物没有污染,且释放大量能量,有一定应用前景。氨气燃烧生成水和另一种气体,该气体占空气的体积分数约为78%。请写出氨气燃烧反应的化学方程式_________________________。
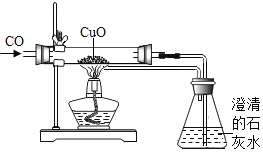
【题目】某校化学硏究性学习小组的成员,他们在查阅资料时,发现单质碳能够在高温时与金属氧化物反应得到金属单质。于是,他们用木炭与CuO进行了如下的探究活动请你参与他们的这次活动,并解决有关问题。
(提出问题)
木炭与氧化铜反应除生成单质铜外,还生成什么呢?
(猜想与假设)
(1)可能是CO
(2)可能是CO2
(设计方案)
为了检验CO,他们设计的方案是:把小动物放在收集的气体中,观察能否存活。后经充分研究后,认为此方案不可行,其不可行的理由是_________。
(査阅资料)
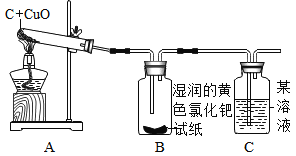
将滤纸浸泡在磷钼酸和氯化钯的黄色混合溶液中制成的试纸遇CO立即变成蓝色,而遇CO2不变色。
实验现象 | 实验结论 |
A中固体由黑色变成_________ | 有铜生成 |
B中黄色试纸没有变蓝 | 没有_______生成 |
C中__________ | 有CO2生成 |
(实验与结论)
设计的实验装置图如下:
(反思与评价)
(1)对于下列三种氧化铜和炭粉的质量比,你建议选择_______(填序号)的比例,你选择的理由是_________。
A 42:3 B 40:3 C 38:3
(2)根据上述实验及学习的木炭与氧化铜、氧化铁的反应,请你归纳出单质碳的一项重要用途是_________。写出焦炭还原氧化铁的化学方程式________。
【题目】将乙醇和氧气置于密闭容器中引燃,测得反应前后各物质的质量如下:
物质(纯净物) | 乙醇 | 氧气 | 二氧化碳 | 水 | M |
反应前质量/g | 2.3 | 4 | 0 | 0 | 0 |
反应后质量/g | 0 | 0 | 2.2 | X | Y |
表格中“X、Y”分别为_____;若要使生成物中无物质M,需要再增加氧气的质量为_____g。