题目内容
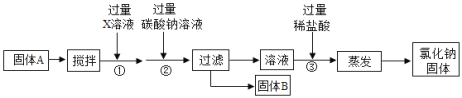
【题目】下图为探究金属化学性质的两组实验。
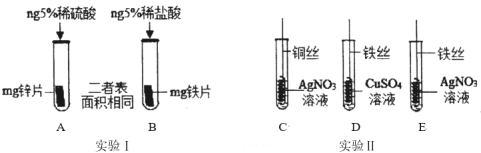
(1)实验Ⅰ中以“金属表面产生气泡的快慢”为标准来判断锌、铁的活动性强弱,小萍同学认为该实验设计不够合理,理由是_____________________________________________________。
(2)写出实验Ⅱ中C试管内反应的化学方程式________________________________________。
(3)实验Ⅱ中要验证Cu、Fe、Ag的金属活动性顺序,至少要做的实验是_____(填字母序号)。若实验室只有铜片,小明将铜片分别放入两种盐溶液中,也通过实验验证了三种金属的活动性顺序,所用的两种盐溶液是_____________和____________(填化学式)。
【答案】酸的种类不同 Cu+2AgNO3═Cu(NO3)2+2Ag CD FeSO4溶液 AgNO3溶液
【解析】
(1)从图可以看出选取的酸的种类不同,因此以“金属表面产生气泡的快慢”为标准来判断锌、铁的活动性强弱不够合理;
(2)由图示可知,实验Ⅱ中C试管内的反应是铜与硝酸银反应生成了硝酸铜和银,实验现象是红色铜丝表面有银白色物质、溶液由无色变为蓝色,反应的化学方程式为:Cu+2AgNO3═Cu(NO3)2+2Ag;
(3)由图示可知,在C中铜能置换出硝酸银中的银,说明活动性铜>银,在D中的铁能置换出硫酸铜中的铜,说明活动性铁>铜,所以可得活动性:铁>铜>银,用于证明铁、铜、银的金属活动性顺序实验是:CD;小华将铜片分别放入两种溶液中,也通过实验验证了三种金属的活动性顺序,由“三取中”的方法可知,所用的两种溶液是:FeSO4溶液和AgNO3溶液。

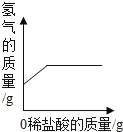
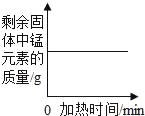
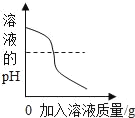
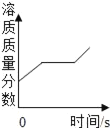
【题目】下表所述各实验过程中某些量之间的变化关系,其中正确的是( )
① | ② | ③ | ④ |
向一定量铁粉中滴加稀盐酸 | 加热一定量高锰酸钾固体 | 向稀盐酸中滴加过量的氢氧化钠溶液 | 将硝酸钾不饱和溶液恒温蒸发水分,直至有晶体析出 |
|
|
|
|
A. 只有①B. 只有②C. ①、②、④D. ②、③、④