题目内容
某CuO粉末中混有少量Cu2O,现有一课外活动小组利用下图所示装置测定其中Cu2O的含量,请根据图示内容回答下列问题: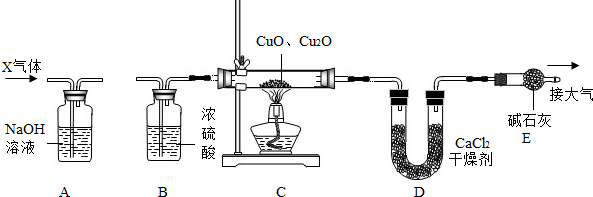
(1)X是常见还原性气体CO、H2中的一种,请根据组合装置判断X的化学式为
(2)B装置的作用是
(3)已知Cu2O在加热的条件下也能被X气体还原为Cu,写出该反应的化学方程式:
(4)已知反应前CuO和Cu2O的总质量为m1g,完全反应后U型管内物质的质量增加了m2g(损失忽略不计),则原混合物中Cu2O的质量为
(5)E装置的作用是
(6)若进入C中的气体换成两种气体中的另外一种,同样要求用该装置完成Cu2O含量的测定实验,则D中的药品应改换为
分析:氢气具有还原性,能够还原氧化铜和氧化亚铜;氢氧化钠溶液能够吸收酸性氧化物;浓硫酸能吸收水;氯化钙固体能吸收水;碱石灰能吸收水和二氧化碳;根据化学方程式可以进行相关方面的计算.
解答:解:(1)如果是一氧化碳,则还原氧化物后生成的二氧化碳气体不能被氯化钙吸收,所以应该是氢气.故填:H2;
A装置的作用是除去X气体中可能混有的酸性气体.故填:除去X气体中可能混有的酸性气体.
(2)B装置的作用是除去X气体中的水蒸气;故填:除去X气体中的水蒸气;
若缺少B装置,将直接导致反应后D装置内的物质的质量有偏大.故填:D.
(3)氢气还原氧化亚铜的化学方程式为:H2+Cu2O
2Cu+H2O.
(4)解设氧化亚铜的质量为X,则氧化铜的质量为m1g-X.
H2+Cu2O
2Cu+H2O;H2+CuO
Cu+H2O
144 18 80 18
X
m1g-X m2g-
80:18=( m1g-X):(m2g-
)
X=(2.25m1-10m2)g.
答:氧化亚铜的质量为(2.25m1-10m2)g.
(5)E装置的作用是吸收空气中的水蒸气.故填:吸收空气中的水蒸气.
(6)碱石灰能够吸收反应生成的二氧化碳气体.故填:碱石灰.
A装置的作用是除去X气体中可能混有的酸性气体.故填:除去X气体中可能混有的酸性气体.
(2)B装置的作用是除去X气体中的水蒸气;故填:除去X气体中的水蒸气;
若缺少B装置,将直接导致反应后D装置内的物质的质量有偏大.故填:D.
(3)氢气还原氧化亚铜的化学方程式为:H2+Cu2O
| ||
. |
(4)解设氧化亚铜的质量为X,则氧化铜的质量为m1g-X.
H2+Cu2O
| ||
| ||
144 18 80 18
X
| 18X |
| 144 |
| 18X |
| 144 |
80:18=( m1g-X):(m2g-
| 18X |
| 144 |
X=(2.25m1-10m2)g.
答:氧化亚铜的质量为(2.25m1-10m2)g.
(5)E装置的作用是吸收空气中的水蒸气.故填:吸收空气中的水蒸气.
(6)碱石灰能够吸收反应生成的二氧化碳气体.故填:碱石灰.
点评:解答本题要掌握各种物质的性质和相关方面的计算方法,只有这样才能对问题做出正确的判断.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目



