题目内容
 (2012?历下区二模)如图1所示,实验室制取并收集满一瓶C02后,向瓶中倒入澄清石灰水,迅速用预先绑好一个小气球的橡皮塞塞紧.
(2012?历下区二模)如图1所示,实验室制取并收集满一瓶C02后,向瓶中倒入澄清石灰水,迅速用预先绑好一个小气球的橡皮塞塞紧.(1)振荡装置,可以观察到小气球
膨胀
膨胀
(填“膨胀”、“缩小”、“无变化”之一),简述出现该现象的原因二氧化碳与氢氧化钙反应消耗气体,导致瓶内的压强小于大气压
二氧化碳与氢氧化钙反应消耗气体,导致瓶内的压强小于大气压
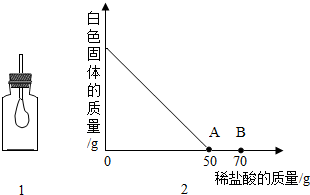
(2)实验后,过滤出瓶中白色固体放入烧杯,向烧杯中逐滴滴加溶质质量分数为1.46%的稀盐酸,烧杯中白色固体的质量与所滴入稀盐酸的质量关系曲线如图所示.请根据题意回答下列问题:
①当滴入1.46%的稀盐酸70g时(即图2中B点),烧杯中溶液所含的溶质是:
HCl,CaCl2
HCl,CaCl2
(填化学式)②当滴入1.46%的稀盐酸50g时(即图2中A点),烧杯中所得不饱和溶液的质量.(计算结果保留到O.Olg)
分析:根据已有的知识进行分析,二氧化碳能与氢氧化钙反应生成碳酸钙沉淀和水,气体被消耗,则密闭容器内的压强变小,碳酸钙能与盐酸反应生成氯化钙、水和二氧化碳,格局反应的量,即可计算所得溶液的质量.
解答:解:(1)二氧化碳能与氢氧化钙反应生成碳酸钙和水,二氧化碳被消耗,则瓶内的压强小于大气压,在大气压的作用下,小气球会膨胀,故填:膨胀,二氧化碳与氢氧化钙反应消耗气体,导致瓶内的压强小于大气压;
(2)碳酸钙能与盐酸反应生成氯化钙、水和二氧化碳,当加入70g盐酸时,碳酸钙已经完全反应,盐酸过量,故溶液中含有的溶质是氯化钙和氯化氢,故填:HCl,CaCl2;
(3)当滴入1.46%的稀盐酸50g时,碳酸钙和盐酸恰好完全反应,设碳酸钙的质量是x,生成的二氧化碳的质量是y,则有
CaCO3+2 HCl=CaCl2+H2O+CO2↑
100 73 44
x 1.46%×50g y
=
=
x=1g y=0.44g
所得溶液的质量为:1g+50g-0.44g=50.56g
答:所得不饱和溶液的质量为50.56g.
(2)碳酸钙能与盐酸反应生成氯化钙、水和二氧化碳,当加入70g盐酸时,碳酸钙已经完全反应,盐酸过量,故溶液中含有的溶质是氯化钙和氯化氢,故填:HCl,CaCl2;
(3)当滴入1.46%的稀盐酸50g时,碳酸钙和盐酸恰好完全反应,设碳酸钙的质量是x,生成的二氧化碳的质量是y,则有
CaCO3+2 HCl=CaCl2+H2O+CO2↑
100 73 44
x 1.46%×50g y
| 100 |
| x |
| 73 |
| 1.46%×50g |
| 44 |
| y |
x=1g y=0.44g
所得溶液的质量为:1g+50g-0.44g=50.56g
答:所得不饱和溶液的质量为50.56g.
点评:本题考查了氢氧化钙与二氧化碳的反应以及与物理压强知识的结合和根据化学方程式的计算,完成此题,可以依据已有的知识结合图示进行.

练习册系列答案
相关题目