题目内容
现有四种含铁化合物:①FeO;②Fe2O3;③Fe3O4;④FeS,其含铁元素的质量分数由大到小的排列顺序为_____(填序号,下同);相同质量的①磷②硫③铁④镁在氧气中燃烧时消耗氧气的质量由小到大的排列顺序为_____;铝在氧气中燃烧的化学方程式为:_____。
 阅读快车系列答案
阅读快车系列答案下列方案可达实验目的的是(_______)
选项 | 实验目的 | 实验方案 |
A | 鉴别热固性塑料和热塑性塑料 | 取样,灼烧闻气味 |
B | 鉴别氯化钾和氯化铵 | 取样,分别加氢氧化钙研磨,闻气味 |
C | 除去氯化钠溶液中的氢氧化钠 | 加入过量的稀硫酸 |
D | 比较铝和铜的活动性强弱 | ____________ |
小组同学查资料知道泡沫灭火器原理是:AlCl3+3NaHCO3=3NaCl +Al(OH)3↓+3CO2↑
(提出问题)此反应发生的原因是否由于AlCl3呈酸性?
(实验)测定AlCl3溶液的酸碱性
(1)用__________测定溶液的酸碱性。
(提出问题)NH4Cl溶液呈酸性,它是否也能与NaHCO3溶液反应?
(实验)按下图1进行实验:
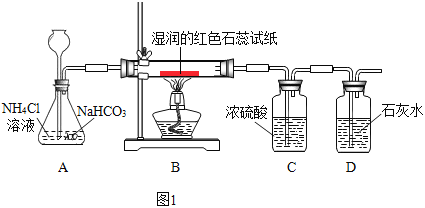
观察到的现象是:湿润的红色石蕊试纸变蓝,石灰水变浑浊
(2)C中浓硫酸的作用是________,D中石灰水的作用是_______。
(3)A中的反应化学方程式是_________。
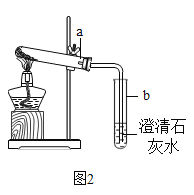
(实验反思)Ⅰ、Na2CO3和 NaHCO3 的性质区别
按图2进行实验:取适量的NaHCO3 粉末加到a试管中,加热,观察到a试管口有水生成,b试管中澄清石灰水变浑浊。持续加热直至两试管均不再发生变化时,发现a试管中仍残留有较多白色固体粉末。
(4)小文猜测白色固体粉末可能是:①NaOH;②Na2CO3;③NaCl.小燕认为猜想③一定不正确,理由是_______,小燕从试管内取少量白色固体溶于水,滴加酚酞,溶液变红,她判断该固体为NaOH,小美认为她的实验设计不合理,因为_________。
(5)他们继续探究固体成分,设计了如下实验:
操作步骤 | 实验现象 | 结论 |
取少量白色固体于试管中,加水溶解,向其中滴加足量_______溶液 | ______ | 剩余的固体有Na2CO3 |
静置,继续滴加酚酞 | 不变红 | 剩余的固体没有NaOH |
通过实验证明: 2NaHCO3  Na2CO3+ CO2↑ + H2O,NaHCO3热稳定性较Na2CO3差。
Na2CO3+ CO2↑ + H2O,NaHCO3热稳定性较Na2CO3差。
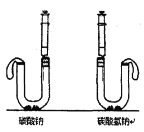
Ⅱ、泡沫灭火器中应用
(6)按如图进行实验:U型管中分别加入等质量碳酸钠和碳酸氢钠固体,在两支注射器中分别吸入同溶质质量分数、同体积的足量稀盐酸,然后同时迅速将盐酸分别注入U型管中。____边U型管乳胶套膨胀更大,等质量碳酸钠和碳酸氢钠与盐酸反应生成的气体质量比是____________。


 点燃酒精灯 B.
点燃酒精灯 B. 滴加液体
滴加液体 移走蒸发皿 D.
移走蒸发皿 D. 读出液体的体积
读出液体的体积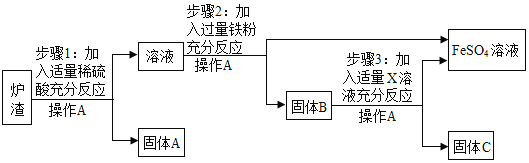
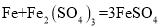 ,另一个反应的化学方程式为:_____。
,另一个反应的化学方程式为:_____。