��Ŀ����
����Ŀ������Һ�н����Ƶô�����Fe��OH��2 �� ԭ����Fe��OH��2���ȶ�����ˮ��ֻҪ��һ�������ͼ���Ӧ���ɺ��ɫ����Fe��OH��3 �� 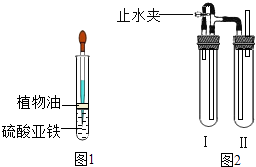
д���䷴Ӧ�Ļ�ѧ����ʽ�� ��
���������־�����Ƶķ��������Ƶð�ɫ��Fe��OH��2������
����һ��
�ò�������������ˮ����FeSO4��Һ��NaOH��Һ��Ȼ��Ӧ�Ʊ���
a����ȥ����ˮ���ܽ���������������ķ�����
b����ͼ��ʾ���ó��ι���ȡ����O2��NaOH��Һ������FeSO4��ҺҺ���£��ټ���NaOH��Һ���Թ����Ͳ�������� ��
��������
����ͼ2װ�����Ʊ���
a��װ�æ��м���Fe��ϡH2SO4 �� д���䷴Ӧ�Ļ�ѧ����ʽ����װ�â��м���NaOHŨ��Һ��
bΪ���Ƶð�ɫFe��OH��2��������Ҫ���в��裬��˳��Ϊ
�������Լ�� �������鴿 �ۼ����Լ�������Ƥ�� �ܴ�ֹˮ�� �ݼн�ֹˮ�У�
c��д���Թܢ��з����Ļ�ѧ��Ӧ����ʽ�� �� �������ɵ�Fe��OH��2�����ܽϳ�ʱ�䱣�ְ�ɫ��
���𰸡�4Fe��OH��2+O2+2H2O�T4Fe��OH��3�����ȣ��������������������ĸ��ţ�Fe+H2SO4�TFeSO4+H2�����٢ۢܢڢݣ�FeSO4+2NaOH�TFe��OH��2��+Na2SO4��H2SO4+2NaOH�TNa2SO4+2H2O����H2SO4+Fe��OH��2�TFeSO4+2H2O��
���������⣺����Fe��OH��2���ȶ�����ˮ�У�ֻҪ��һ�������ͼ�������Ӧ����Fe��OH��3 �� ���Ƴ���Ӧ��ΪFe��OH��2��ˮ������������ΪFe��OH��3������ż����ƽ������ʽ��4Fe��OH��2+2H2O+O2�T4Fe��OH��3�� ����һ��a������������ܽ�����¶ȳɷ��ȣ�������м��ɽ�ˮ�е�������ȥ��b��ע��ֲ���ͷ�ֹ�������������룻��3���ó��ι���ȡ����O2��NaOH��Һ������FeSO4��ҺҺ����Ҳ��Ϊ�˷�ֹ�������������룻
��������a��Fe��ϡH2SO4��Ӧ���������������������Ѿ�ƽ�ˣ�ע���������ŵı귨��b���й��������ȡ������Ҫ���װ�õ������ԣ���������װ���м����Լ����������ӣ���ֹˮ�У�����������������װ�â�Ҫ����װ�â��п����Ƿ��ž���Ҫ��װ�âܿڼ�������Ĵ��ȣ������崿�����ر�ֹˮ�У�������ѹ����ʹ���е�ҩƷ������У�����е�ҩƷ��Ӧ�õ�������������c�������������ᷴӦ�������������������ܻ���û��Ӧ�������������������������Ӧ�������������������������ƣ��������������ᷴӦ���������ƺ�ˮ��������������������Ӧ��������������ˮ��
���Դ��ǣ�4Fe��OH�� 2+O2+2H2O�T4Fe��OH��3������һ��a�����ȣ�b���������������������ĸ��ţ���������a��Fe+H2SO4�TFeSO4+H2����b���٢ۢܢڢݣ�c��FeSO4+2NaOH�TFe��OH��2��+Na2SO4����д����H2SO4+2NaOH�TNa2SO4+2H2O ����H2SO4+Fe��OH��2�TFeSO4+2H2O����
�����㾫����ͨ��������ý������ϵ�ѡ�����ݺ���д��ѧ����ʽ�����ֱ���ʽ�����뷽��ʽ�����պ�ɫ������ͨ��ָ�����̡��������ǵĺϽ��ؽ�������ͭ��п��Ǧ�ȣ���ɫ��������������ơ�þ�����ȣ���ɫ������ͨ����ָ����ɫ�������������������ע�⣺a����ƽ b������ c�����ż����Խ����⣮