题目内容
【题目】(1)物质的性质决定物质的用途,反之物质的用途又反映物质的性质。请填写下列空格。
①氮气化学性质不活泼,可用作___________________;
②石墨具有_________,可用于制作干电池的电极;
③由于一氧化碳具有____________,可用于冶炼金属;
④由于活性炭具有吸附性,可用于除去水中的_____________。
(2)能源与环境成为人们日益关注的问题。
①目前人们利用最多的能源是煤、_________________和天然气等化石燃料。为使燃料充分燃烧,减少污染,可采用的方法除提供充足的氧气外,还可_________________________。
②氢化镁(MgH2)固体可作为氢动力汽车的能源提供剂。提供能源时MgH2与水反应生成氢氧化镁和氢气,该反应的化学方程式为______________。
【答案】 保护气 导电性 还原性 异味和色素 石油 增大与氧气的接触面 MgH2+2H2O ![]() Mg(OH)2+2H2↑
Mg(OH)2+2H2↑
【解析】(1)①氮气化学性质不活泼,可用作食品保护气;
②石墨可用于制作干电池的电极,说明具有导电性;
③一氧化碳具有还原性,可用于冶炼金属;
④由于活性炭具有吸附性,可用于除去水中的异味和色素;
(2)①化石燃料包括煤、石油、天然气,为了使燃料充分燃烧,可以采取的方法有:足够的氧气、增大燃料与氧气的接触面积;
②MgH2与水反应生成氢氧化镁和氢气,反应的化学方程式为:MgH2+2H2O═Mg(OH)2+2H2↑。

 53随堂测系列答案
53随堂测系列答案【题目】浴室喷头长时间使用会有白色固体附着,俗称水垢。这是因为硬水中含有较多的可溶性的碳酸氢钙【Ca(HCO3)2】,还含有可溶性的碳酸氢镁【Mg(HCO3)2】。查阅资料,加热时会产生难溶性的固体。其中碳酸氢钙【Ca(HCO3)2】受热易分解,生成难溶性的化合物、气体等物质。某小组想探究碳酸氢钙受热分解后产物的成分。
【提出猜想】猜想1.难溶性化合物可能是CaCO3;猜想2.气体可能是H2、CO、CO2 。
【方案设计】请你设计实验,帮助该组同学确定难溶物的成分。
实验步骤 | 实验现象 | 结论 |
_____ | _______ | 难溶物是CaCO3 |
【实验探究】该组同学设计如图实验,继续探究气体的成分。
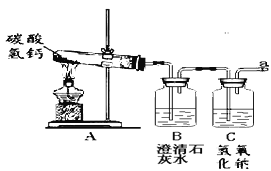
操作1.加热A装置,一段时间后,B装置中的澄清石灰水变浑浊。
操作2.在a处用燃着的木条检验,无明显现象。
【实验结论】结论1.碳酸氢钙分解产生的气体是____________;
结论2.碳酸氢钙受热分解的化学方程式为_____________________________。
【反思评价】有同学提出:硬水中可溶性的碳酸氢镁【Mg(HCO3)2】受热也会产生不溶性的固体,那水垢的成分中还有什么物质?根据上述探究,该组同学设计如下图装置进一步实验。(已知碱石灰主要成分为CaO和NaOH)
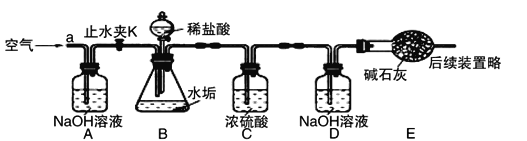
【实验测定】 步骤如下:
①按图组装仪器,先_____________,再将50g水垢样品放入锥形瓶中。
②打开止水夹K,从导管a处缓缓鼓入一定量的空气。
③逐滴加入足量稀盐酸,待锥形瓶中出现气泡不再产生现象时,停止滴加稀盐酸。
④打开止水夹K,从导管a处缓缓鼓入一定量的空气;
⑤称量D瓶内物质增加的质量,直至D瓶内物质质量不变;
⑥测量滴加稀盐酸体积与D瓶内物质增加质量的关系如下图曲线所示。
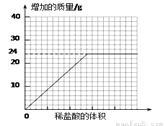
【讨论交流】
①A装置中的NaOH溶液的作用是____________________,若没有A装置,D装置中的质量将_______________(填“偏大”、“不变”或“偏小”)。
②C装置中浓硫酸的作用是__________________,E装置的作用是____________________。
③分析曲线图,通过计算可知:水垢中一定含有(化学式)________,理由是________________。
④查阅资料:水垢的主要成分有CaCO3、MgCO3和Mg(OH)2三种成分,三种物质加热后均能生成两种氧化物。小组同学提出探究水垢中氢氧化镁的质量分数:另取质量为50g的水垢试样,放入试管中加热至质量不再减少为止,测得二氧化碳24 g,残留固体25.1g。结合以上数据,确定水垢样品中氢氧化镁的质量分数为_______________。(结果保留小数点后一位)
【题目】下列物质的归类正确的是
选项 | 甲 | 乙 |
A | 无机材料 | 陶瓷、玻璃、青铜 |
B | 同一物质 | 烧碱、纯碱、苛性钠 |
C | 提供能量营养物 | 淀粉、蛋白质、无机盐 |
D | 常见干燥剂 | 浓硫酸、生石灰、石灰石 |
A. A B. B C. C D. D