题目内容
【题目】根据题目要求填空。
(1)洁净的空气对于人类非常重要,下列做法不利于保护大气的是(________)
A.使用洁净能源 B.节日燃放烟花 C.植树造林 D.取消公交车,多开私家车
(2)为了保护大气,2011年11月在我国新颁布的《环境空气质量标准》中,基本监控项目增设了可吸入颗粒物的浓度限值,与该监测项目有关的是___。
A.二氧化氮 B.一氧化碳 C.PM2.5 D.臭氧
(3)现有下列物质:A.过氧化氢;B.铜;C.澄清石灰水;D.液态空气;E.高锰酸钾;F.稀有气体;G.铁丝;H浮在水面上的冰;请在以下空格中填写上述有关物质的序号:
①属于化合物的是______;②属于混合物的是______; ③属于含氧化合物,但不属于氧化物的是______.
(4)完成下列符号的书写:
A.空气中含量第二的元素和地壳中含量最高的金属元素组成的化学式______
B.相对分子质量最小的气体的化学式_____
C.电子数为10的原子团离子______
D.既能表示某种元素,又能表示某种物质的符号_____
(5)元素周期表是学习研究化学的重要工具.下表是1~18号元素的部分最高正化合价和最低负化合价规律信息:
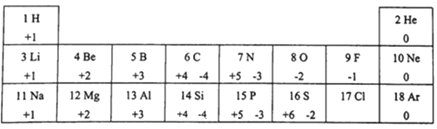
请分析信息并回答下列问题:
①12号元素属于______元素(填“金属”或“非金属”),它的离子与______(写元素符号)原子具有相同的核外电子数.
②推断17号元素最高正化合价为____,其最低负化合价与Si形成化合物的化学式为____.
(6)利用物质沸点不同可以实现混合物的分离,根据下表数据判断。
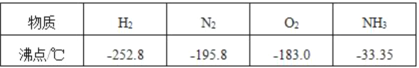
要将工业合成氨的产物氨气(NH3)从它的反应物氮气和氢气的混合物中分离开来,最适宜的温度应该控制在___℃<T<___℃,该过程属于_______(填物理/化学)变化。
(7)烟道气体脱硫可以有效地治理燃煤带来的环境污染。脱硫方法有多种,世界普遍使用的是钙法,所占比例在90%以上。某钙法脱硫工艺的主要反应是:
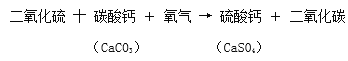
其中碳酸钙在自然界中主要存在于大理石、石灰岩和贝壳等物质中。
①上述反应涉及的物质中,属于单质的是_______(写名称)。
②在将SO2转化为CaSO4的过程中,硫元素的化合价____(填“升高”、“降低”或“不变”)。
③该脱硫工艺的优点是______。
(8)水是生命之源,也是人类最宝贵的资源。用你学过的化学知识回答下列问题:
①自然界中的水都不是纯水,净水时需加入明矾的目的是___________ 。
②欲除去水中不溶性杂质,需进行过滤操作,该操作过程中玻璃棒所起的作用是______。
③某同学在完成电解水实验时,发现正极产生了10 mL气体,则负极产生的气体体积是 ____。该实验能够说明水是由氢元素与氧元素组成的理论依据是 ___。
【答案】BD C AEH CDF E Al2O3 H2 OH- He 金属 Ne +7 SiCl4 -195.8 -33.35 物理 氧气 升高 能消除有害气体,不生成新的污染物;原料易得,成本低 吸附沉降 引流 20mL 化学反应前后元素种类不变
【解析】
(1)A、使用洁净能源可以减少污染物的排放,有利于保护大气;B、燃放烟花会生成有害气体和粉尘,不利于保护大气;C、植树造林会净化空气,有利于保护大气;D、取消公交车,多开私家车,易造成空气污染,不有利于保护大气;
(2)与PM2.5项目监测项目有关的是可吸入颗粒物;
(3)①由两种或两种以上的元素组成的纯净物叫化合物,过氧化氢、高锰酸钾、在水面上的冰都属于化合物;②混合物是由两种或两种以上的物质组成,澄清石灰水、液态空气、稀有气体都属于混合物;③氧化物是指由两种元素组成的化合物中,其中一种元素是氧元素,高锰酸钾属于含氧化合物,但不是氧化物;
(3)A、空气中含量第二的元素是氧元素,地壳中含量最高的金属元素是铝元素,二者组成的物质的化学式为Al2O3;
B、相对分子质量最小的气体是氢气,化学式:H2;
C、电子数为10的原子团离子是氢氧根离子,符号为:OH-;
D、既能表示某种元素,又能表示某种物质的可以是氦气,符号为:He;
(5)①12号元素是镁元素,属于金属元素;镁原子核外电子排布情况为2、8、2结构,在化学反应中易失去最外层的2个电子,形成2、8结构,与氖原子结构相同;
②17号元素是氯元素,核外有17个电子,最高价与最外层电子数相同,即+7价,最低价为-1价,硅元素显+4价,形成的化合物的化学式为SiCl4;
(6)氨气、氮气、氢气的沸点分别为-33.35℃、-195.8℃、-252℃,要将工业合成氨的产物氨气(NH3)从它的反应物氮气和氢气的混合物中分离开来,应该采取剩余氨气,也就是让氨气不气化,最适宜的温度应该控制在-195.8~-33.35℃.该过程中没有新物质生成,属于物理变化;
(7)①二氧化硫(SO2)+碳酸钙+氧气→硫酸钙(CaSO4)+二氧化碳,属于单质的是氧气;
②烟道气体脱硫中的“硫”指的是硫元素;②SO2中硫元素的化合价为+4价,CaSO4中硫元素的化合价+6价;将SO2转化为CaSO4的过程中,硫元素的化合价升高;
③该脱硫工艺的优点是能消除有害气体,不生成新的污染物;原料易得,成本低;
(8)①由于明矾溶于水生成的胶状物具有吸附性,所以,自然界中的水都不是纯水,净水时需加入明矾的目的是吸附沉降;
②欲除去水中不溶性杂质,需进行过滤操作,该操作过程中玻璃棒所起的作用是引流;
③某同学在完成电解水实验时,正负极的气体之比为1:2,发现正极产生了10mL气体,则负极产生的气体体积是20mL;该实验能够说明水是由氢元素与氧元素组成的理论依据是化学反应前后元素种类不变。

【题目】实验是化学学科的重要特征之一。
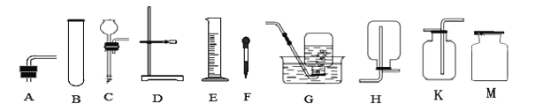
(1)实验室部分装置如 A~D 所示。完成下表空格。
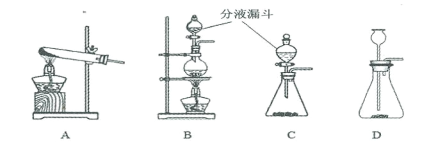
制取的气体 | 反应物 | 反应条件 | 反应装置(填字母) |
①O2 | 氯酸钾固体 | 二氧化锰固体、加热 | ______ |
②CO2 | 大理石和稀盐酸 | 常温 | ____或_____ |
③N2 | 氯化铵溶液和NaNO2溶液 | 加热 | _______ |
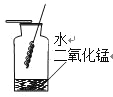
(2)用排水法收集氧气的原因是 ___。如图所示是铁丝在氧气中燃烧的改进实验。用适量H2O2溶液和MnO2代替原实验中集气瓶里的水,其优点除了使实验更简便外,还有 ___。
(3)已知:常温下,氮气沸点为-196℃,氧气沸点为-183℃。将燃着的木条置于盛满液态空气的烧杯口,观察到的现象是 ____,该烧杯放置一段时间后,液态物质剩余约 1/10 体积,其主要成分是______(填 化学式)。
(4)如图是有关氧气的知识结构图(部分反应条件省略,参加反应的氧气为足量),请回答下列问题
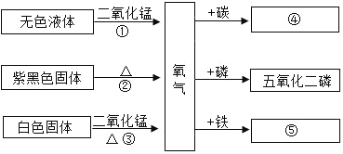
写出反应③的文字表达式为 ___。你还学习过哪些物质能与氧气反应?请写出一个反应的文字表达式 ___。