题目内容
【题目】两种固体物质(均不含结晶水)的溶解度曲线如图所示。下列说法正确的是
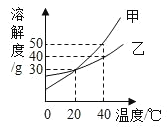
A.0℃时,甲的溶解度大于乙的溶解度
B.0℃时,等质量的甲、乙溶液中溶质质量一定相等
C.将 40℃时乙的饱和溶液降温至 20℃,仍然是饱和溶液
D.将甲的饱和溶液转化为不饱和,溶质质量分数不可能减小
【答案】C
【解析】
A、通过分析溶解度曲线可知,0℃时,甲的溶解度小于乙的溶解度,故A错误;
B、0℃时,等质量的甲、乙溶液的状态不能确定,所以溶液中溶质质量不能确定,故B错误;
C、乙的溶解随温度的降低而减小,将40℃时乙的饱和溶液降温至20℃,溶解度减小,析出晶体,所以仍然是饱和溶液,故C正确;
D、将甲的饱和溶液转化为不饱和,增加溶剂的方法可使溶质质量分数减小,故D错误。
故选:C。

 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案【题目】小林同学在体育课上腿部擦伤,医务室的大夫在她伤口上涂了医用过氧化氢溶液,小林看到伤口处产生了小气泡,很好奇。为什么瓶中的过氧化氢溶液涂到伤口上,分解就加快了呢?
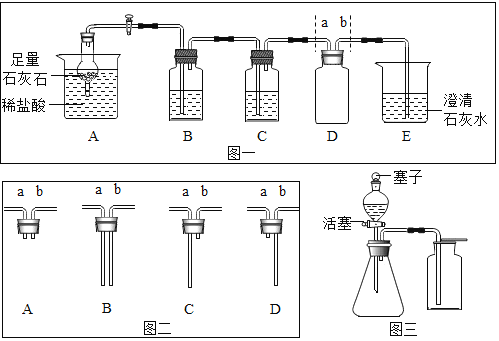
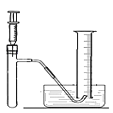
(1)小林准备用如图所示装置测定过氧化氢分解的快慢,实验前在注射器中吸入过氧化氢溶液,量筒内装满水。实验开始时,向试管中注入过氧化氢溶液,并用排水法收集氧气,记录2分钟收集的气体体积。请写出过氧化氢分解的反应方程式:_____________。
(2)小林查阅了相关资料,并进行了探究实验
(查阅资料)
①过氧化氢是人体代谢废物之一,它能够对机体造成损害,人体存在过氧化氢酶,可以催化过氧化氢分解。
②温度对化学反应的快慢有影响,人体正常体温是37℃。
(提出猜想)
猜想1:过氧化氢分解加快是因为体温比瓶中的温度高。
猜想2:过氧化氢分解加快是因为伤口中有过氧化氢酶。
(进行实验)
序号 | 实验步骤 | 实验现象 | 实验结论 |
① | 分两次进行实验,均注入5mL过氧化氢溶液 第一次在常温下进行 第二次将试管浸在37℃的温水中 | 量筒中2分钟收集到的气体体积均为5mL | 。 |
② | 分两次进行实验 第一次将装有一小粒过氧化氢酶的试管浸在37℃的温水中,注入5mL过氧化氢溶液 第二次 | 第一次,量筒中2分钟收集到的气体体积为56 mL 第二次,量筒中2分钟收集到的气体体积为 | 过氧化氢分解加快是因为过氧化氢酶的作用 |
a.实验①结论是_____________ 。
b.实验②中横线部分应进行的操作是____________。
c.实验②中第二次收集到的氧气体积为__________。
(实验反思)
小林反思了实验过程,认为人体中过氧化氢酶是在体温条件下发挥作用的,实验得出的结论可能存在不足。因此又补充进行了几组实验,数据记录如下表所示。
d.通过这些数据,你能得出的新结论是______________。
加入过氧化氢酶 | 不加过氧化氢酶 | |||||
反应温度/℃ | 25 | 37 | 42 | 25 | 37 | 42 |
收集到气体体积/mL | 39 | 56 | 34 | 5 | 5 | 5 |