题目内容
【题目】白云石粉是一种生产高级玻璃器皿、医药用瓶、光学玻璃的原料,某化学兴趣小组对白云石粉极其好奇,决定对其进行探究。
【查阅资料】
白云石属于碳酸盐矿物,白云石粉主要成分的化学式可表示为xMgCO3·yCaCO3 ( 杂质是二氧化硅,其不溶于水,也不与盐酸反应,受热不分解)
一、定性探究:白云石粉的成分和性质
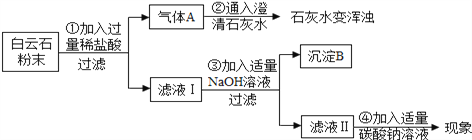
【实验分析】
(1)由步骤①②的现象可得出白云石粉中一定含有的离子是_________ (填离子符号)。
(2)步骤③生成氢氧化镁的化学方程式是________;步骤④的反应现象是_______。
【结论】综合上述实验现象可初步证明白云石由碳酸钙、碳酸镁组成。
【实验质疑】小组同学经过讨论认为:因氢氧化钙微溶于水,导致沉淀B中除了氢氧化镁之外应该还混有氢氧化钙,对定量测定白云石粉的组成干扰较大,在老师的指导下该兴趣小组采用热分解法进行定量探究。
二、定量探究:白云石的组成
【查阅资料】碳酸钙开始分解的温度为898℃,1000℃时完全分解生成生石灰和二氧化碳气体;碳酸钙与碳酸镁的化学性质相似;碳酸镁开始分解的温度为540℃,700℃时完全分解。
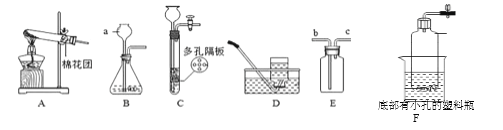
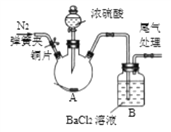
【实验设计】为测定白云石中的含钙量及x:y的值,该兴趣小组设计了如下装置并进行实验:

【实验步骤】
①组装仪器,检查装置的气密性;
②准确称取15.0g 白云石粉末放在A装置中,打开弹簧夹,鼓入一段时间氮气,称量B、C、D、E装置的质量;
③关闭弹簧夹,打开控温电加热器,缓缓调升温度至700℃,持续加热至固体质量不变;
④打开弹簧夹,缓缓鼓入一段时间氮气,准确称量B、C、D、E装置的质量;
⑤关闭弹簧夹,调升温度至1000℃,持续加热至固体质量不变,打开弹簧夹,缓缓鼓入一段时间氮气,准确称量B、C、D、E装置的质量。
实验数据记录如表:
B中溶液质量/g | C中溶液质量/g | D中溶液质量/g | E的质量/g | |
反应前 | 50.0 | 100.0 | 50.0 | 120.5 |
700℃ | 50.0 | 102.1 | 50.1 | 120.5 |
1000℃ | 50.0 | 106.3 | 50.3 | 120.5 |
【实验分析和数据处理】
(3)装置D的作用是______________________。
(4)持续加热至固体质量不变后缓缓鼓入一段时间氮气的目的是__________。
(5)计算白云石中钙元素的质量分数______。(写出计算过程,结果保留小数点后一位,)
(6)设计实验证明白云石粉已完全分解的实验方法是 ______(写出实验方法、现象、结论)
(7)白云石(xMgCO3·yCaCO3)中的 x:y=________ (最简整数比),若加热前没有鼓入一段时间的氮气,将会导致 x:y的值___________(填偏大、偏小或不变).
【答案】 ![]()
![]() ═
═![]() ↓
↓![]() 产生白色沉淀 吸收氮气带出的水蒸气,防止测得二氧化碳的质量偏小 使残留在装置内的二氧化碳气体全部被C装置吸收 26.7% 取少量反应后固体于试管中,加入足量的稀盐酸,无气泡产生,说明完全分解 1:2 偏大
产生白色沉淀 吸收氮气带出的水蒸气,防止测得二氧化碳的质量偏小 使残留在装置内的二氧化碳气体全部被C装置吸收 26.7% 取少量反应后固体于试管中,加入足量的稀盐酸,无气泡产生,说明完全分解 1:2 偏大
【解析】本题通过白云石粉研究,考查了实验探究物质的组成成分以及含量,过滤的原理、方法及其应用;常见气体的检验与除杂方法,盐的化学性质,书写化学方程式和根据化学反应方程式的计算。综合性较强,解题是时要充分利用“查阅资料”弄清碳酸钙和碳酸镁的分解顺序,为数据处理提供依据。
(1)碳酸根离子能和氢离子结合成水和二氧化碳,因此由步骤①②的现象可得出白云石粉中一定含有的离子是CO32-;
(2)步骤③中,氯化镁和氢氧化钠反应生成白色沉淀氢氧化镁和氯化钠,反应的化学方程式为:MgCl2+2NaOH═Mg(OH)2↓+2NaCl;氯化钙能和碳酸钠反应生成白色沉淀碳酸钙和氯化钠,实验现象是产生白色沉淀;
(3)气体从装置C出来的气体中含有少量的水蒸气。装置D的作用是吸收氮气带出的水蒸气,防止测得二氧化碳的质量偏小;
(4)持续加热至固体质量不变后缓缓鼓入一段时间氮气的目的是使残留在装置内的二氧化碳气体全部被C装置吸收;
(5)设碳酸钙的质量为x,
碳酸钙分解生成二氧化碳质量=(106.3g-102.1g)+( 50.3g-50.1g)=4.4g,
CaCO3![]() CaO+CO2↑
CaO+CO2↑
100 44
x 4.4g
![]() x=10g,
x=10g,
ω(Ca)═(10g×40%)/15g═26.7%;
(6)若白云石粉已完全分解反应后固体中没有碳酸钙和碳酸镁,可用稀盐酸检验。实验证明白云石粉已完全分解的实验方法是:取少量反应后固体于试管中,加入足量的稀盐酸,无气泡产生,说明完全分解;
(7)设碳酸镁质量为y,
碳酸镁分解生成二氧化碳的质量=(102.1g-100.0g)+(50.1g-50.0)=2.2g,
MgCO3![]() MgO+CO2↑,
MgO+CO2↑,
84 44
y 2.2g
![]() y=4.2g,
y=4.2g,
根据题意有:84x:100y=4.2g:10g x:y=1:2;若加热前没有鼓入一段时间的氮气,导致测得的碳酸镁分解生成的二氧化碳质量偏大,从而会导致x:y的值偏大。

 阅读快车系列答案
阅读快车系列答案【题目】某化学兴趣小组有一次活动的内容是:对一包干燥的红色粉末组成进行探究。请你参与并回答有关问题。
【教师提醒】:它由Cu、Fe2O3、Fe(OH)3三种固体中的一种或两种组成。
【提出猜想:】红色粉末可能的组成有: ①只有Cu;②只有Fe2O3;③只有Fe(OH)3;④是Fe2O3、Fe(OH)3的混合物;⑤是Cu、Fe2O3的混合物;⑥是Cu、Fe(OH)3的混合物。
【资料获悉】:
(1)氢氧化铁受热分解为氧化铁和水。(2)白色无水硫酸铜遇水变蓝。
(3)氧化铁可以和稀盐酸反应生成氯化铁和水。
(4)铜在黄色氯化铁溶液中可以发生反应生成氯化亚铁和氯化铜。
【探究思路】:利用物质的性质不同设计实验加以甄别,先分别探究其中是否含有Fe(OH)3, Cu等,逐步缩小范围,然后再选择适当的试剂和方法通过实验探究其组成。 (装置内空气中的水蒸气、二氧化碳忽略不计)
【实验探究】:
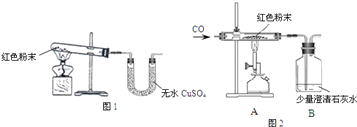
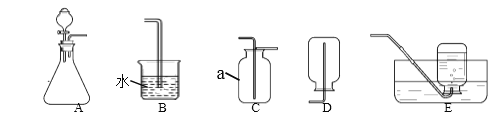
(1)甲同学取适量红色粉末装入试管中,按图1进行实验。结果无水硫酸铜没有变蓝,从而排除猜想中的_________。(填猜想中的序号)
(2)在甲同学实验结论的基础上,乙同学另取少量红色粉末于试管中,滴加足量稀盐酸,振荡后观察,发现固体全部溶解,溶液变色。乙同学认为可以排除猜想中的①和⑤,而丙同学认为只能排除猜想①,你认为_________的观点正确(填"乙"或"丙")。
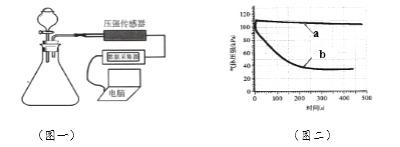
(3)丁同学为进一步确定红色粉末的组成,称取5.0g该粉末装入硬质玻璃管中,按图2在通风橱中进行实验.开始时缓缓通入CO气体,过一段时间后再加热使其充分反应。待反应完全后,停止加热,仍继续通CO气体直至玻璃管冷却。反应前后称量相关装置和物质的总质量,其数据如下表:
组别 | 反应前 | 反应后 |
Ⅰ组 | 玻璃管和红色粉末总质量为37.3g | 玻璃管和固体物质总质量为36.1g |
Ⅱ组 | 洗气瓶和所盛溶液总质量为180.0g | 洗气瓶和物质总质量为183.1g |
【交流讨论】:
(1)在装置中先通CO气体的作用是________。
(2)应该选择_________组的实验数据计算来确定红色粉末的组成。最终计算结果表明:该红色粉末的组成是猜想中的第_________组(填序号)。
(3)实验中观察到A装置中的现象为___________。
(4)为了防止溶液倒吸,本实验停止加热前是否需要先断开A和B的连接处?_______(填"需要"或"不需要"),理由是________。
【反思评价】:从环保角度,图二缺少尾气处理装置。