题目内容
【题目】某校化学兴趣小组同学发现,长期使用的热水壶底部有一层水垢,水垢的主要成分是碳酸钙.他们为了测定水垢中碳酸钙的含量,将足量盐酸加入到12.5g水垢中,产生CO2气体的情况如图所示. 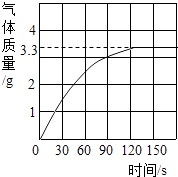
(1)从图中可以看出,12.5g水垢与足量盐酸反应后生成的CO2最多是g.
(2)水垢中碳酸钙的质量分数是多少?
【答案】
(1)3.3
(2)解:设12.5g水垢中碳酸钙的质量为 x
CaCO3+2HCl═CaCl2+H2O+ | CO2↑ |
100 | 44 |
X | 3.3g |
![]() =
= ![]() ,解得x=7.5g
,解得x=7.5g
水垢中碳酸钙的质量分数为: ![]() ×100%=60%
×100%=60%
答:水垢中碳酸钙的质量分数是60%
【解析】解:(1)从该题的图中我们看到起点为0点,说明装置内原先没有气体,折点和终点在同一水平线,说明最终制得气体的质量相等且为3.3g;所以答案是:3.3;
【考点精析】本题主要考查了根据化学反应方程式的计算的相关知识点,需要掌握各物质间质量比=系数×相对分子质量之比才能正确解答此题.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】下列对分子、原子、离子的认识,正确的是( )
A. 原子是最小的粒子,不可再分
B. 氮分子是保持氮气化学性质的最小微粒
C. 原子得到电子,带正电,变为阳离子
D. 固体难压缩,说明固体分子间无间隔
【题目】小明在做“盐酸中和氢氧化钠”的实验时,实验前忘记向氢氧化钠溶液中滴加酚酞溶液,导致无法判断中和反应进行的程度,于是小明对反应后溶液的酸碱性进行了探究. 【探究目的】确定反应后溶液的酸碱性
(1)【猜想与假设】反应后溶液呈碱性,也可能呈 , 也可能呈 .
(2)【实验验证】
实验操作 | 实验现象 | 实验结论 |
| 无色酚酞溶液; | 溶液呈碱性,使其呈碱性的微粒是; |
无色酚酞溶液不变色 | 溶液呈; |
(3)【继续验证】
实验操作 | 实验现象 | 实验结论 |
| 粉末部分或全部消失,溶液变为黄色 | 溶液呈 , 反应的化学方程式是; |
溶液呈; |