题目内容
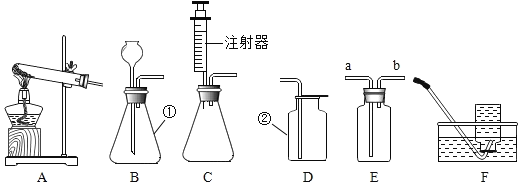
【题目】下图所示为实验室中常见的气体制备和收集装置。
请回答下列问题:
(1)写出图中标示的仪器名称:①是_______________, ②是________________。
(2)实验室用高锰酸钾制取氧气,应选用发生装置____________(填字母序号)。若用装置D收集氧气,验满的方法是______________________。
(3)实验室用过氧化氢溶液和二氧化锰制取氧气,若选用C做发生装置,你认为选用C的优点是__________________。
(4)由于二氧化碳的密度比空气____________,欲使用装置 E用排空气法收集二氧化碳, 则气体应从__________(填“a” 成“b”)端通入,欲使用装置E用排水法收集氧气,先将瓶中装满水,再将气体从______________ (填“a” 或“b”)端通入。
(5)已知一氧化氮气体难溶于水,在空气中容易与氧气发生反应,则收集一氧化氮气体时应选用图中装置____________(填字母序号);
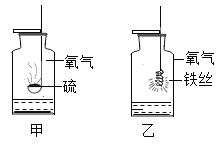
(6)下图是检验氧气性质的两个实验。其中实验甲的集气瓶中预先加入了少量水,其作用是______;实验乙观察到的现象是____________,反应的化学方程式是__________。
【答案】锥形瓶 集气瓶 A 用带火星的木条放在集气瓶口,若木条复燃证明氧气已集满 能控制反应的速率 大 a b F 吸收二氧化硫气体,防止污染空气 剧烈燃烧,火星四射,放出大量的热,生成一种黑色固体 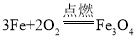
【解析】
高锰酸钾加热生成锰酸钾、二氧化锰和氧气,过氧化氢在二氧化锰催化作用下生成水和氧气,铁在氧气中点燃生成四氧化三铁。
(1)图中标示的仪器名称:①是锥形瓶, ②是集气瓶。
(2)高锰酸钾加热生成锰酸钾、二氧化锰和氧气,实验室用高锰酸钾制取氧气,反应需要加热,故应选用发生装置A。若用装置D收集氧气,氧气具有助燃性,故验满的方法是用带火星的木条放在集气瓶口,若木条复燃证明氧气已集满。
(3)实验室用过氧化氢溶液和二氧化锰制取氧气,若选用C做发生装置,C装置含有注射器,可以控制过氧化氢溶液的滴加速率和滴加量,进而控制反应速率,故选用C的优点是能控制反应的速率。
(4)由于二氧化碳的密度比空气大,欲使用装置 E用排空气法收集二氧化碳,二氧化碳气体从长管通入,空气从短管排出,则气体应从a端通入,欲使用装置E用排水法收集氧气,先将瓶中装满水,氧气密度比水小,氧气从短管通入,故再将气体从b端通入。
(5)一氧化氮气体难溶于水,在空气中容易与氧气发生反应,选用排水法收集,则收集一氧化氮气体时应选用图中装置F。
(6)二氧化硫有毒且易溶于水,所以集气瓶底预先加入少量水的作用是吸收二氧化硫气体,防止污染空气,故实验甲的集气瓶中预先加入了少量水,其作用是吸收二氧化硫气体,防止污染空气;铁在氧气中点燃生成四氧化三铁,故实验乙观察到的现象是剧烈燃烧,火星四射,放出大量的热,生成一种黑色固体,反应的化学方程式是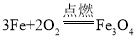 。
。

【题目】2020年初,新型冠状病毒疫情爆发。一定浓度的乙醇、过氧化氢、过氧乙酸(CH3COOOH)、次氯酸钠(NaClO)等溶液能有效杀灭病毒。
(1)乙醇、过氧化氢、过氧乙酸、次氯酸钠中,属于有机化合物的是乙醇和__________。
(2)用作消毒剂的医用酒精中乙醇的体积分数为75%,就是指每100体积的医用酒精中含__的乙醇。大面积喷洒医用酒精易引发火灾,请写出乙醇完全燃烧的化学方程式:______。
(3)实验室常采用分解过氧化氢的方法制取氧气,化学方程式为_______。
质量分数为30%、5%的过氧化氢溶液以及水的密度见下表:
液体 | 质量分数为30%的过氧化氢溶液 | 质量分数为5%的过氧化氢溶液 | 水 |
密度 | 1.1g/cm3 | 1.0g/cm3 | 1.0g/cm3 |
要把50mL质量分数为30%的过氧化氢溶液稀释为质量分数为5%的过氧化氢溶液,需要水的体积为__________mL。
(4)利用次氯酸钠发生器,通过电解食盐水能够制得次氯酸钠溶液,该反应的化学方程式为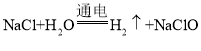 。请分析该反应中各元素化合价的变化:_______。
。请分析该反应中各元素化合价的变化:_______。