题目内容
(5分)某研究性学习小组为探究镁与水的反应,设计如下实验:
步骤1:将镁条用砂纸打磨至光亮,分成两等份。
步骤2:将一份光亮的镁条置于冷水中,几乎没有观察到任何现象。
步骤3:将另一份光亮的镁条置于热水中,观察到有气泡产生。
(1)将镁条用砂纸打磨至光亮的原因是 。
(2)经百度可知,活泼金属与水反应生成对应的碱和氢气,如果金属活动性越强,生成的碱的碱性越强。某同学就向步骤3的烧杯中滴加酚酞试液,观察到镁条的表面有明显的红色出现。该反应的化学方程式: ,反应类型是 (基本反应类型)。
(3)步骤2和3对比可知,影响镁与水的反应速率的一个因素是 。
(4)根据以上信息,若将金属钠加到硫酸铜溶液中,可能观察到的现象是 。
练习册系列答案
相关题目
下列除去杂质的方法正确的是
选项 | 物质 | 杂质 | 除杂方法 |
A | CaCl2溶液 | 稀盐酸 | 加入过量的CaCO3,过滤 |
B | 盐酸 | 硫酸 | 加入过量BaCl2溶液,过滤 |
C | NaNO3 | NaCl | 加入过量AgNO3溶液,过滤 |
D | CaO | Ca(OH)2 | 加过量水,过滤 |
A. A B. B C. C D. D



 、
、 、
、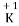 、
、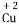 、
、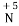 ,请选择元素,写出符合要求的化合物的化学式:
,请选择元素,写出符合要求的化合物的化学式: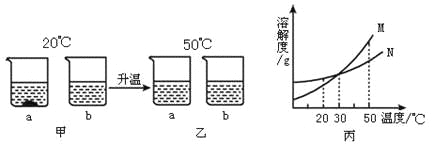
 称量固体氢氧化钠 B.
称量固体氢氧化钠 B.  测溶液pH
测溶液pH 配制溶液 D.
配制溶液 D.  稀释浓硫酸
稀释浓硫酸