题目内容
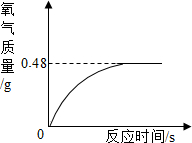 (1)小军从家中拿来一瓶久置的医用过氧化氢溶液,和同学们一起测定.他们从瓶中取出该溶液共51g,加入适量二氧化锰,生成氧气的质量与反应时间的关系如图所示:则该溶液中所含双氧水的实际质量是多少克?
(1)小军从家中拿来一瓶久置的医用过氧化氢溶液,和同学们一起测定.他们从瓶中取出该溶液共51g,加入适量二氧化锰,生成氧气的质量与反应时间的关系如图所示:则该溶液中所含双氧水的实际质量是多少克?(2)已知蔗糖的化学式为C12H22O11.计算:
①它的相对分子质量是多少?
②蔗糖中碳元素的质量分数是多少?
考点:根据化学反应方程式的计算,相对分子质量的概念及其计算,元素的质量分数计算
专题:化学式的计算,有关化学方程式的计算
分析:(1)根据图象可知生成氧气的质量,然后根据过氧化氢溶液分解的化学方程式和生成气体的质量,列出比例式,即可计算出参与反应的H2O2的质量;
(2)
①根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答.
②根据化合物中元素的质量分数=
×100%,进行分析解答.
(2)
①根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答.
②根据化合物中元素的质量分数=
| 相对原子质量×原子个数 |
| 相对分子质量 |
解答:解:
(1)由图象可知生成氧气的质量为0.48g
设51g过氧化氢溶液中含过氧化氢的质量为x.
2H2O2
2H2O+O2↑
68 32
x 0.48 g
=
x=1.02g
该溶液中所含双氧水的实际质量为1.02 g
(2)
①蔗糖的相对分子质量为为12×12+1×22+16×11=342.
②蔗糖中碳元素的质量分数=
×100%≈42.1%.
答案:
(1)该溶液中所含双氧水的实际质量为1.02 g
(2)
①它的相对分子质量是342;②蔗糖中碳元素的质量分数是42.1%.
(1)由图象可知生成氧气的质量为0.48g
设51g过氧化氢溶液中含过氧化氢的质量为x.
2H2O2
| ||
68 32
x 0.48 g
| 68 |
| 32 |
| x |
| 0.48g |
x=1.02g
该溶液中所含双氧水的实际质量为1.02 g
(2)
①蔗糖的相对分子质量为为12×12+1×22+16×11=342.
②蔗糖中碳元素的质量分数=
| 12×12 |
| 342 |
答案:
(1)该溶液中所含双氧水的实际质量为1.02 g
(2)
①它的相对分子质量是342;②蔗糖中碳元素的质量分数是42.1%.
点评:本题主要考查学生运用化学方程式和溶质的质量分数公式进行计算的能力.考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
现有H2S、S、R、CuSO4四种物质,是按硫元素的化合价由低到高排列的,其中R这种物质的化学式可能是( )
| A、Na2S2O3 |
| B、Ag2SO4 |
| C、K2S |
| D、K2SO4 |
下列物质的用途不正确的是( )
A、 液氮作冷冻麻醉 |
B、 氮气作闪光灯 |
C、 二氧化碳作肥料 |
D、 氧气用于炼钢 |
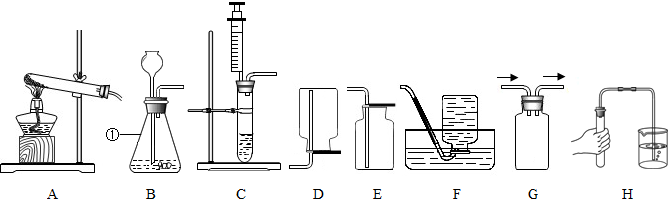
 碳元素是组成许多物质的基本元素.
碳元素是组成许多物质的基本元素.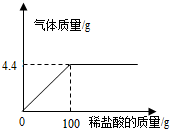 化学探究小组为测定石灰石样品中碳酸钙的质量分数,取15g样品放入烧杯,然后逐滴加入一定质量分数的盐酸反应(杂质不溶于水也不参与反应),加入的酸与生成气体的关系如下.请完成:
化学探究小组为测定石灰石样品中碳酸钙的质量分数,取15g样品放入烧杯,然后逐滴加入一定质量分数的盐酸反应(杂质不溶于水也不参与反应),加入的酸与生成气体的关系如下.请完成: