题目内容
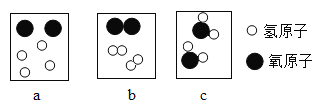
【题目】由A和B两种元素组成的化合物中,已知A和B的元素质量比为21:8,而A和B的相对原子质量之比为7:2,则该化合物的化学式为( )
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
【答案】B
【解析】
要确定这种化合物的化学式,必须确定元素A、B在化合物中原子个数关系,可通过假设原子个数的方法,利用所给的数据计算出两元素的原子个数比,最后完成化学式的推断。
设化合物的化学式为AaBb,则元素A的相对原子质量为7M时,元素B的相对原子质量为2M;化合物AaBb中X、Y两元素的质量比=(7M×a):(2M×b)=7a:2b,根据题意:化合物中A、B两元素的质量比为21:8,则7a:2b=21:8 ,解得a:b=3:4,则这种化合物的化学式为A3B4。
故选:B。

练习册系列答案
相关题目
【题目】学习了二氧化锰对过氧化氢有催化作用的知识后。某同学想:氧化铜能否起到类似二氧化锰的催化剂作用呢?于是进行了如下探究。
(猜想)Ⅰ.氧化铜不是催化剂、也不参与反应,反应前后质量和化学性质不变;
Ⅱ.氧化铜参与反应产生氧气,反应前后质量和化学性质发生了改变;
Ⅲ.氧化铜是反应的催化剂,反应前后_____和_____不变。
(实验)用天平称量0.2g氧化铜,取5mL 5%的过氧化氢溶液于试管中,进行如下实验:
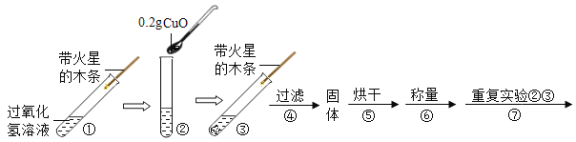
(1)填写下表:
步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
_____, 带火星的木条复燃 | 所得固体 _____g | 溶液中有气泡放出, _____ | 猜想Ⅰ、Ⅱ不成立 猜想Ⅲ成立 |
(2)步骤①的目的是_____。
(3)过氧化氢能被氧化铜催化分解放出氧气的化学反应的文字表达式为_____。