题目内容
金属与酸的反应(分别写出镁、铝、锌、铁与稀盐酸和稀硫酸反应的方程式)| 稀盐酸 | 稀硫酸 | |
| 镁 | ||
| 铝 | ||
| 锌 | ||
| 铁 |
【答案】分析:金属与酸的反应(分别写出镁、铝、锌、铁与稀盐酸和稀硫酸反应的方程式):
知道反应的快慢速度与金属活动性有关,生成的气体能够燃烧,并且产生淡蓝色火焰;且燃烧生成的产物为水,证明该气体为氢气;金属与酸的反应为置换反应,符合A(单质)+BC=C(单质)+AB,故可以实现化学方程式.
解答:解:由题意知:反应物、生成物,根据质量守恒定律,正确书写化学方程式;如镁与盐酸反应:反应物为镁与盐酸,生成物为氯化镁与氢气,根据质量守恒定律,故正确书写化学方程式Mg+2HCl=MgCl2+H2↑;同理,可知其他反应的反应物和生成物,以及各化学方程式的书写.
故答为:
点评:根据题目信息,找出反应物和生成物,再利用书写化学方程式的方法及步骤,根据质量守恒定律,正确书写化学方程式;掌握金属的化学性质和置换反应的概念及其应用.
知道反应的快慢速度与金属活动性有关,生成的气体能够燃烧,并且产生淡蓝色火焰;且燃烧生成的产物为水,证明该气体为氢气;金属与酸的反应为置换反应,符合A(单质)+BC=C(单质)+AB,故可以实现化学方程式.
解答:解:由题意知:反应物、生成物,根据质量守恒定律,正确书写化学方程式;如镁与盐酸反应:反应物为镁与盐酸,生成物为氯化镁与氢气,根据质量守恒定律,故正确书写化学方程式Mg+2HCl=MgCl2+H2↑;同理,可知其他反应的反应物和生成物,以及各化学方程式的书写.
故答为:
| 稀盐酸 | 稀硫酸 | |
| 镁 | Mg+2HCl=MgCl2+H2↑ | Mg+H2SO4=MgSO4+H2↑ |
| 铝 | 2Al+6HCl=2AlCl3+3H2↑ | 2Al+3H2SO4=Al2(SO4)3+3H2↑ |
| 锌 | Zn+2HCl=ZnCl2+H2↑ | Zn+H2SO4=ZnSO4+H2↑ |
| 铁 | Fe+2HCl=FeCl2+H2↑ | Fe+H2SO4=FeSO4+H2↑ |
点评:根据题目信息,找出反应物和生成物,再利用书写化学方程式的方法及步骤,根据质量守恒定律,正确书写化学方程式;掌握金属的化学性质和置换反应的概念及其应用.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
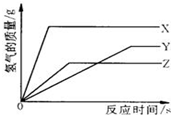 某校化学活动小组为探究X、Y、Z三种金属与酸的反应情况,进行了如下实验,取等质量的X、Y、Z分别与足量的溶质质量分数相同的稀H2SO4反应,都生成+2价金属的硫酸盐,反应情况如图所示,下列对该图象理解的叙述中,正确的是( )
某校化学活动小组为探究X、Y、Z三种金属与酸的反应情况,进行了如下实验,取等质量的X、Y、Z分别与足量的溶质质量分数相同的稀H2SO4反应,都生成+2价金属的硫酸盐,反应情况如图所示,下列对该图象理解的叙述中,正确的是( )