题目内容
【题目】如图是某品牌葡萄糖酸锌口服液的标签,请根据标签信息回答下列问题。

(1)葡萄糖酸锌是由_____种元素组成的。
(2)葡萄糖酸锌的相对分子质量为_____。
(3)这支口服液中含锌元素的质量为_____。
【答案】4 455 6.5mg
【解析】
(1)由葡萄糖酸锌的化学式就可知道它由几种元素组成;
(2)根据相对分子质量等于各元素的相对原子质量×个数之和,计算即可。
(3)根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答。
(1)由葡萄糖酸锌的化学式可知,它由碳、氢、氧、锌4种元素组成。故答案为:4。
(2)葡萄糖酸锌的相对分子质量为:12×12+1×22+16×14+65=455,故答案为:455。
(3)这支口服液中含锌元素的质量为45.5mg×![]() ×100%=6.5mg,故答案为:6.5mg。
×100%=6.5mg,故答案为:6.5mg。

【题目】金属用途广泛,其结构和性质等是化学的重要研究内容。
(1)下图是铝的原子结构示意图。下列说法不正确的是_____。
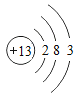
A 铝原子的质子数为13 B 在化合物中铝通常显+3价
C 铝是地壳中含量最多的元素 D 铝可作导线是由于它具有良好的导电性
(2)某化学小组用一定量AgNO3和Cu(NO3)2混合溶液进行了下图实验,并对溶液A和固体B的成分进行了分析和实验探究。
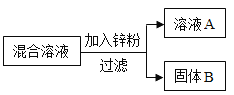
(提出问题)溶液A中的溶质可能有哪些?
(作出猜想)①只有Zn(NO3)2②Zn(NO3)2、AgNO3③Zn(NO3)2、Cu(NO3)2④Zn(NO3)2、AgNO3、Cu(NO3)2
(交流讨论)不合理的猜想是_____(填标号),其理由是_____。
(实验探究)若猜想①成立,通过以下实验可确定固体B的成分,请将下表填写完整。
实验步骤 | 现象 | 有关反应的化学方程式 |
取少量固体B,滴加_____ | 有气泡产生 | _____ |
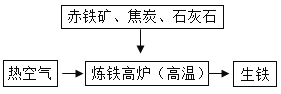
(3)下图是工业炼铁示意图。其中,焦炭的作用是燃烧提供能量和_____;有铁生成的化学方程式为_____。
(4)某工厂利用废铁屑与废硫酸起反应来制取硫酸亚铁。现有废硫酸49t(H2SO4的质量分数为10%),与足量废铁屑起反应,可生产硫酸亚铁的质量是_____