题目内容
 请根据如图所示实验回答问题.
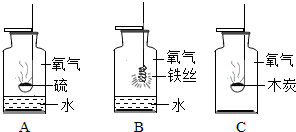
请根据如图所示实验回答问题.(1)A装置中,水的作用
(2)B装置中,铁丝在氧气中燃烧时观察到的现象是
(3)如C装置所示.①做木炭在氧气中燃烧的实验时,操作的方法是:把加热到红热的木炭由瓶口
分析:(1)根据二氧化硫有毒且能溶于水分析;
(2)根据铁丝燃烧的现象和化学方程式的书写方法分析;
(3)根据木炭燃烧时的注意事项和二氧化碳的性质分析.
(2)根据铁丝燃烧的现象和化学方程式的书写方法分析;
(3)根据木炭燃烧时的注意事项和二氧化碳的性质分析.
解答:解:(1)集气瓶底部留少量水的作用是吸收生成的二氧化硫,防止污染空气,故答案为:吸收生成的二氧化硫,防止污染空气;
(2)铁在纯氧中燃烧的现象是:剧烈燃烧、火星四射、放出热量、生成黑色固体;氧气与铁反应生成的四氧化三铁,配平即可.故答案为:剧烈燃烧、火星四射、放出热量、生成黑色固体;3Fe+2O2
Fe3O4;
(3)做木炭在氧气中燃烧的实验时,为防止氧气受热扩散,正确的操作应是从上到下慢慢插入,使之与氧气充分接触木;往集气瓶里加入少量的澄清石灰水,振荡,若澄清的石灰水变浑浊,则证明发生了化学反应,故答案为:向下慢慢;往集气瓶里加入少量的澄清石灰水,振荡,若澄清的石灰水变浑浊,则证明发生了化学反应.
(2)铁在纯氧中燃烧的现象是:剧烈燃烧、火星四射、放出热量、生成黑色固体;氧气与铁反应生成的四氧化三铁,配平即可.故答案为:剧烈燃烧、火星四射、放出热量、生成黑色固体;3Fe+2O2
| ||
(3)做木炭在氧气中燃烧的实验时,为防止氧气受热扩散,正确的操作应是从上到下慢慢插入,使之与氧气充分接触木;往集气瓶里加入少量的澄清石灰水,振荡,若澄清的石灰水变浑浊,则证明发生了化学反应,故答案为:向下慢慢;往集气瓶里加入少量的澄清石灰水,振荡,若澄清的石灰水变浑浊,则证明发生了化学反应.
点评:本题主要考查了氧气的化学性质,氧气的化学性质也是中考的重要考点之一,要在理解的基础上加强记忆.

练习册系列答案
相关题目
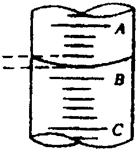
 某同学用如图所示的装置在实验室加热高锰酸钾制取氧气,请回答问题:
某同学用如图所示的装置在实验室加热高锰酸钾制取氧气,请回答问题: 某同学用如图所示的装置在实验室加热高锰酸钾制取氧气,请回答问题:
某同学用如图所示的装置在实验室加热高锰酸钾制取氧气,请回答问题:

