题目内容
【题目】现有含杂质的氯化镁样品10g(杂质不溶于水,也不参加反应),向其中加入一定量的氢氧化钠溶液恰好完全反应,过滤,得到117g质量分数为10%的溶液.求:
①样品中氯化镁的质量分数;
②所加入氢氧化钠溶液的质量分数(计算结果精确到0.1%).
【答案】解:117g质量分数为10%的溶液中氯化钠的质量是:117g×10%=11.7g
设样品中氯化镁的质量为x,消耗氢氧化钠的质量为y
MgCl2+2NaOH═Mg(OH)2↓+2NaCl
95 80 117
x y 11.7g![]()
![]() x=9.5g
x=9.5g![]()
![]() y=8g
y=8g
①样品中氯化镁的质量分数是![]()
![]() =95%;
=95%;
②据质量守恒定律可知氢氧化镁的质量是:9.5g+8g﹣11.7g=5.8g
氢氧化钠溶液的质量=117g+5.8g﹣9.5g=113.3g
则加入的氢氧化钠溶液中溶质的质量分数为:![]()
![]() =7.1%
=7.1%
答:①样品中氯化镁的质量分数为95%;②氢氧化钠溶液中溶质的质量分数为7.1%.
【解析】本题容易出错的地方是氢氧化钠溶液质量的计算,可根据质量守恒定律分析,并了解混合物中物质的质量分数,溶质的质量分数计算方法,结合题意分析解答即可.

【题目】实验探究题
请根据下列实验装置图(如图甲所示)回答问题。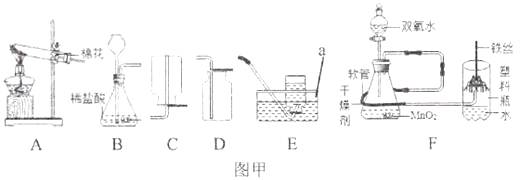
(1)写出仪器a的名称:。
(2)用A装置制取O2的化学方程式为 , 若需要干燥的氧气,则应选用的收集装置为 (填装置编号)。
(3)图F是“铁丝在氧气中燃烧”实验的改进装置。
①气体发生装置中发生反应的化学方程式为。
②实验时,打开分液漏斗活塞,通入干燥氧气约10秒,引燃铁丝,伸入塑料瓶内,并对准玻璃管口正上方。改进后的优点有 (填字母)。
A.氧气无需提前制备和收集,操作更方便
B.铁丝的燃烧不再需要火柴引燃
C.装置集氧气的制取、干燥和性质验证于一体,实验更优化
(4)硫化氢是有毒气体,能溶于水形成氢硫酸(其化学性质与盐酸相似),某同学用块状硫化亚铁(FeS)和稀盐酸在常温下发生复分解反应制H2S时。
①应选择图甲中的发生装置 (填字母)来制取H2S;
②写出该实验室制H2S的化学方程式;
③某同学用图乙所示的装置来收集处理H2S,用化学方程式表示氢氧化钠溶液的作用是。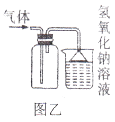
(5)如图丙是测定空气中氧气含量实验的装置图,请结合图示回答有关问题。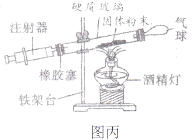
①硬质玻璃管内的固体粉末应选用
A.炭粉B.硫粉C.铜粉D. MnO2
②根据下表提供的实验数据,完成下表
硬质玻璃管中空气的体积 | 反应前注射器中空气体积 | 反应后注射器中气体体积 | 反应所消耗的氧气的体积 | 实验测得空气中氧气的体积分数 |
25mL | 15mL | 7.4mL |
【题目】填写下列空白。
(1)填写元素名称或元素符号
元素名称 | 氯 | _______ | ___________ | ________ |
元素符号 | ___________ | Si | Hg | Ca |
(2)填写下列物质的名称或化学式
物质名称 | _______ | __________ | 氦气 |
化学式 | H2 | CO2 | ________ |