题目内容
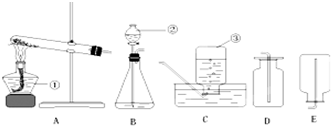
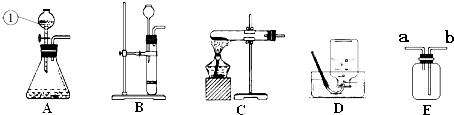
实验室制取氧气时,一般按:
①点燃酒精灯给试管加热;②熄灭酒精灯;③检查气密性;
④把装有高锰酸钾的试管固定在铁架台上;⑤用排水法收集;
⑥将导管移出水面等6步进行的.
其正确的操作顺序是
- A.③④①⑤②⑥
- B.④③①⑤②⑥
- C.④③①⑤⑥②
- D.③④①⑤⑥②
D
用高锰酸钾制取氧气,并以排水集气法收集时,应掌握正确的操作顺序:(1)检查装置的气密性.防止单孔塞与试管口不密合造成漏气而收集不到氧气.(2)加入高锰酸钾,使之平铺在试管底部.(3)按顺序装配仪器,并注意铁夹要夹在离试管口1/3左右处,试管口要略向下倾斜.防止因加热时药品里所含的湿存水变成水蒸气,到管口处冷凝成水滴而倒流,致使试管炸裂.(4)安装好仪器,再点燃酒精灯.加热时,先要把试管均匀预热,然后集中在试管有药品的部位加热,并缓慢地向管底方向移动,使高锰酸钾逐渐分解,氧气平稳放出,便于收集.(5)收集气体时应注意,开始加热时排出的是空气,当气泡连续而均匀地放出时,才是氧气,这时方能收集.(6)在反应结束时应先把导管从水槽中取出,再熄灭酒精灯.如先熄灭酒精灯,试管内温度降低,气压减低,水槽中的冷水会因压力差而被吸入试管,引起试管炸裂.
综上分析,正确的选项是D.
用高锰酸钾制取氧气,并以排水集气法收集时,应掌握正确的操作顺序:(1)检查装置的气密性.防止单孔塞与试管口不密合造成漏气而收集不到氧气.(2)加入高锰酸钾,使之平铺在试管底部.(3)按顺序装配仪器,并注意铁夹要夹在离试管口1/3左右处,试管口要略向下倾斜.防止因加热时药品里所含的湿存水变成水蒸气,到管口处冷凝成水滴而倒流,致使试管炸裂.(4)安装好仪器,再点燃酒精灯.加热时,先要把试管均匀预热,然后集中在试管有药品的部位加热,并缓慢地向管底方向移动,使高锰酸钾逐渐分解,氧气平稳放出,便于收集.(5)收集气体时应注意,开始加热时排出的是空气,当气泡连续而均匀地放出时,才是氧气,这时方能收集.(6)在反应结束时应先把导管从水槽中取出,再熄灭酒精灯.如先熄灭酒精灯,试管内温度降低,气压减低,水槽中的冷水会因压力差而被吸入试管,引起试管炸裂.
综上分析,正确的选项是D.

练习册系列答案
相关题目
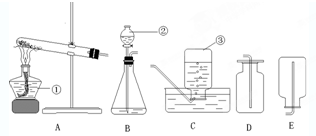 如图是常见的气体发生装置和收集装置.按要求回答问题(所选装置用代号即字母表示)
如图是常见的气体发生装置和收集装置.按要求回答问题(所选装置用代号即字母表示)