题目内容
25g 大理石与盐酸完全反应可制得8.8g的二氧化碳.(友情提示:大理石中的杂质不与盐酸反应).
求:(1)碳酸钙中钙元素、氧元素的质量比是________.
(2)大理石中碳酸钙的质量分数?
解:(1)碳酸钙中钙元素、氧元素的质量比为:40:(16×3)═40:48=5:6 故填:5:6
(2)设碳酸钙的质量为X
CaCO3+2HCl═CaCl2+CO2↑+H2O
100 44
X 8.8g
 =
=
X=20.0 g
大理石中碳酸钙的质量分数是 ×100%=80%
×100%=80%
答:大理石样品中碳酸钙的质量分数为80%
分析:(1)物质中元素的质量比相对原子质量乘以原子个数之比
(2)根据二氧化碳的质量可求出碳酸钙的质量,最后根据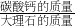 ×100%可求出大理石样品中碳酸钙的质量分数.
×100%可求出大理石样品中碳酸钙的质量分数.
点评:本题主要考查含杂质物质的化学方程式的计算,难度稍大.
(2)设碳酸钙的质量为X
CaCO3+2HCl═CaCl2+CO2↑+H2O
100 44
X 8.8g
 =
=
X=20.0 g
大理石中碳酸钙的质量分数是
 ×100%=80%
×100%=80%答:大理石样品中碳酸钙的质量分数为80%
分析:(1)物质中元素的质量比相对原子质量乘以原子个数之比
(2)根据二氧化碳的质量可求出碳酸钙的质量,最后根据
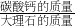 ×100%可求出大理石样品中碳酸钙的质量分数.
×100%可求出大理石样品中碳酸钙的质量分数.点评:本题主要考查含杂质物质的化学方程式的计算,难度稍大.

练习册系列答案
 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案
相关题目