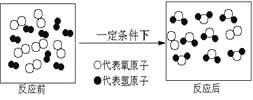
题目内容
【题目】薄荷醇(化学式为C10H20O)可用于糖果、饮料的加香.下列有关薄荷醇的说法正确的是
A. 薄荷醇的相对分子质量为156g
B. 薄荷醇由10个碳原子、20个氢原子和1个氧原子构成
C. 薄荷醇中碳元素、氢元素和氧元素的质量比为10:20:1
D. 薄荷醇中碳元素的质量分数约为76.9%
【答案】D
【解析】
A、相对分子质量单位是“1”,不是“g”,常省略不写,故A错误;B、薄荷醇是由薄荷醇分子构成的,1个薄荷醇分子是由10个碳原子、20个氢原子和1个氧原子构成的,故B错误;C、薄荷醇中碳元素、氢元素和氧元素的质量比为(12×10):(1×20):(16×1)≠10:20:1,故C错误;D、薄荷醇中碳元素的质量分数=![]() ,故D正确。故选D。
,故D正确。故选D。

【题目】小芳发现,氯酸钾与氧化铜混合加热,也能较快产生氧气,于是进行如下探究:
(提出猜想)除MnO2、CuO外,Fe2O3也可以作KClO3分解的催化剂。
(完成实验)按下表进行实验:测定分解温度(分解温度越低,催化效果越好)。
实验编号 | 实验药品 | 分解温度 |
① | KClO3 | 580℃ |
② | KClO3、MnO2(质量比1:1) | 350℃ |
③ | KClO3、CuO(质量比l:1) | 370℃ |
④ | KClO3、Fe2O3(质量比1:1) | 390℃ |
(分析数据、得出结论)
(1)由实验__________与实验④对比,证明猜想合理;
(2)实验所用的三种金属氧化物,催化效果最好的是____________。
(3)若Fe2O3是该反应的催化剂,请写出这个反应的文字表达式___________。
(4)如表是二氧化锰用量与一定质量氯酸钾制取氧气反应速率关系的实验数据。
二氧化锰与氯酸钾的质量比 | 1:40 | 1:20 | 1:10 | 1:5 | 1:3 | 1:2 |
生成1L氧气所需的时间(s) | 124 | 79 | 50 | 54 | 75 | 93 |
①据如表可知二氧化锰与氯酸钾的质量比为_______________时,反应速率最快
②通过分析可知,在化学反应中催化剂的用量____________越多越好 (填“是”或“不是”);
③二氧化锰用量过多冲淡了氯酸钾粉末,相当于减少反应物的________,所以反应速率受到影响。
【题目】如图是化肥碳酸氢铵包装袋上的部分说明,可推测碳酸氢铵具有的性质有_______(填字母)。
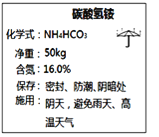
A.易溶于水 B.受热易分解
某同学提出疑问“这种化肥含氮量是否达到16%,化肥中碳酸氢铵的质量分数是多少?”
带着这些问题,该同学进入实验室完成了下列实验。
(查找资料)
①碱石灰能够吸收水和CO2,但是不吸收NH3
②浓硫酸能吸收NH3但是不吸收CO2
③氨气溶于水形成氨水
(性质探究)该同学设计了如下的实验装置:
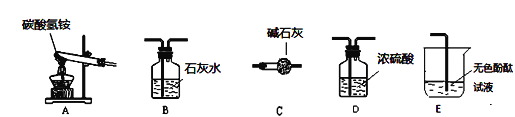
①用A装置给碳酸氢铵加热,装药品前,必须进行的一步操作是_____。
②取适量碳酸氢铵加入试管,连接A、B装置,加热,观察到B中的现象是________。
③再取适量碳酸氢铵加入试管,连接A、C、E装置,加热,E中的现象是__________。
④碳酸氢铵在受热时发生反应的化学表达式是_______。
(含量分析)将装置A、C、D依次连接,加入10g化肥样品,加热至A中固体完全消失。称量装置D的质量如表 (各装置对气体吸收是完全的) :
实验前D装置的质量 | 150.0g |
实验后D装置的质量 | 151.7g |
⑤由此分析得知:反应中产生氨气的质量为__________g。
⑥通过反应的化学表达式可知:氨气中氮元素全部来自于碳酸氢铵(假设杂质中不含氮元素),请计算此化肥中氮元素的质量分数为__________(结果保留到0.1%)。
⑦此化肥中碳酸氢铵的质量分数为__________(结果保留到0.1%)。