题目内容
某电镀厂废水中含有CuSO4、ZnSO4和FeSO4,从废水中回收重要原料硫酸锌和有关金属的流程如下,回答下列有关问题:
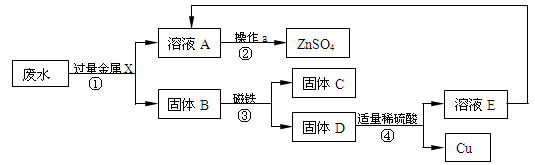
(1)将Fe、Cu、Zn三种金属的活动顺序填入下列空格中:
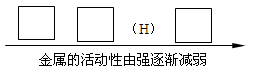
(2)操作a是 。
(3)金属X是 (填化学式),固体B是 (填化学式)。
(4)写出①发生反应的任一个化学方程式 。
(5)①中加入过量的X的目的是 。

(1)将Fe、Cu、Zn三种金属的活动顺序填入下列空格中:

(2)操作a是 。
(3)金属X是 (填化学式),固体B是 (填化学式)。
(4)写出①发生反应的任一个化学方程式 。
(5)①中加入过量的X的目的是 。
(1) (2分,有错漏得0分)
(2分,有错漏得0分)
(2)蒸发(1分) (3)Zn (1分) Zn、Fe、Cu(2分,漏1个得1分,漏2个得0分,错填得0分) (4)Zn+CuSO4===Cu+ZnSO4(或Zn+FeSO4===Fe+ZnSO4,2分) (5)使废液CuSO4、FeSO4中的铜、铁元素全部转化为铜和铁(或使CuSO4、FeSO4全部转化为ZnSO4)(1分)
 (2分,有错漏得0分)
(2分,有错漏得0分) (2)蒸发(1分) (3)Zn (1分) Zn、Fe、Cu(2分,漏1个得1分,漏2个得0分,错填得0分) (4)Zn+CuSO4===Cu+ZnSO4(或Zn+FeSO4===Fe+ZnSO4,2分) (5)使废液CuSO4、FeSO4中的铜、铁元素全部转化为铜和铁(或使CuSO4、FeSO4全部转化为ZnSO4)(1分)
考点:
专题:金属与金属材料.
分析:在金属活动性顺序中,氢前的金属能与酸反应生成氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来.
解答:解:(1)在金属活动性顺序中,锌>铁>氢>铜,所以本题答案为:
(2)要从溶液中得到硫酸锌晶体,可以使用蒸发的方法,所以本题答案为:蒸发;
(3)金属X与废水反应生成的溶液A蒸发后产生硫酸锌晶体,说明加入的金属为锌,锌能与硫酸铜反应生成铜,能与硫酸亚铁反应生成铁,属于固体B中含有多余的锌,反应生成的铜和铁,所以本题答案为:Zn,Zn、Fe、Cu;
(4)锌能与硫酸铜反应生成硫酸锌和铜,能与硫酸亚铁反应生成硫酸锌和铁,任写一个即可,所以本题答案为:Zn+CuSO4═Cu+ZnSO4(或Zn+FeSO4═Fe+ZnSO4 );
(5)加入过量的锌,能将废液中的硫酸铜和硫酸亚铁全部费用生成铜和铁,所以本题答案为:使废液CuSO4、FeSO4中的铜、铁元素全部转化为铜和铁.
点评:本题考查了金属活动性顺序的应用,完成此题,可以依据金属活动性顺序及其意义进行.
专题:金属与金属材料.
分析:在金属活动性顺序中,氢前的金属能与酸反应生成氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来.
解答:解:(1)在金属活动性顺序中,锌>铁>氢>铜,所以本题答案为:

(2)要从溶液中得到硫酸锌晶体,可以使用蒸发的方法,所以本题答案为:蒸发;
(3)金属X与废水反应生成的溶液A蒸发后产生硫酸锌晶体,说明加入的金属为锌,锌能与硫酸铜反应生成铜,能与硫酸亚铁反应生成铁,属于固体B中含有多余的锌,反应生成的铜和铁,所以本题答案为:Zn,Zn、Fe、Cu;
(4)锌能与硫酸铜反应生成硫酸锌和铜,能与硫酸亚铁反应生成硫酸锌和铁,任写一个即可,所以本题答案为:Zn+CuSO4═Cu+ZnSO4(或Zn+FeSO4═Fe+ZnSO4 );
(5)加入过量的锌,能将废液中的硫酸铜和硫酸亚铁全部费用生成铜和铁,所以本题答案为:使废液CuSO4、FeSO4中的铜、铁元素全部转化为铜和铁.
点评:本题考查了金属活动性顺序的应用,完成此题,可以依据金属活动性顺序及其意义进行.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目