题目内容
【题目】现欲探究一固体混合物A的成分,已知其中可能含有BaCl2、Na2CO3、NH4Cl、CuO四种物质中的两种或多种。按下图所示进行实验,出现的现象如图中所示(设过程中所有发生的反应都恰好完全进行):
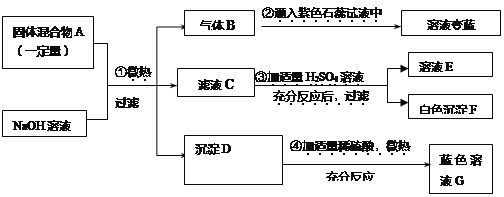
试根据实验过程和发生的现象做出判断,填写以下空白:
⑴气体B有_______________气味。
⑵沉淀F的化学式为_____________。
⑶滤液C中大量存在的溶质有(写化学式)_______________。
⑷混合物A中,肯定不存在的物质是(写化学式)___________,理由是_____________________。
⑸写出实验过程④中发生反应的化学方程式_____________________________________________。
【答案】 刺激性 BaSO4 NaCl、BaCl2 Na2CO3 BaCl2一定存在,若混合物A中存在Na2CO3,在步骤①中会与BaCl2反应,步骤③加入稀硫酸时就不会产生白色沉淀,所以混合物A中肯定不存在Na2CO3 CuO + H2SO4 = CuSO4 + H2O
【解析】 (1).固体与氢氧化钠混合加热,生成能使湿润的红色石蕊试纸变红的气体,所以固体中有氯化铵,氨气有 刺激性 气味。 (2). 氯化钡和硫酸能反应产生白色不溶于酸的沉淀硫酸钡-BaSO4 (3). 滤液C中氢氧化钠和氯化铵反应生成的氯化钠,及样品中原有的氯化钡,NaCl、BaCl2 (4). 固体中一定没有Na2CO3 (5).原因是碳酸钠不与氢氧化钠反应,受热不分解, 而 BaCl2一定存在,若混合物A中存在Na2CO3,在步骤①中会与BaCl2反应,步骤③加入稀硫酸时就不会产生白色沉淀,所以混合物A中肯定不存在Na2CO3 (6). 氧化铜和硫酸反应生成硫酸铜和水,反应的化学方程式 CuO + H2SO4 = CuSO4 + H2O

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】如表物质归类正确的是( )
选项 | 归类 | 物质 |
A | 常见合金 | 生铁、金刚石、青铜 |
B | 复合肥料 | 氯化铵、磷矿粉、硝酸钾 |
C | 化石燃料 | 煤气、石油、天然气 |
D | 常见干燥剂 | 浓硫酸、生石灰、碱石灰 |
A. A B. B C. C D. D



