题目内容
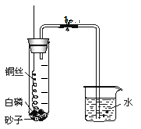
【题目】下图是实验室常用的仪器与装置,回答下列问题。

(1)写出仪器名称:B_________、C_________。
(2)实验室加热高锰酸钾制取氧气,反应的化学方程式为________________。这个实验的发生装置应选用仪器_______________(在A~G中选择)组装,实验时通常在试管口塞一团棉花,作用是______________________。
(3)用H装置收集一瓶干燥的氧气,气体从_________(填“a”或“b”)端进入。
(4)利用如图的装置,可以粗略测定出空气中氧气的体积分数。实验过程如下:
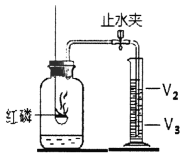
第1步: 在一个容积为V毫升的集气瓶中加入V1毫升(少量)的水,量筒中预先装入V2毫升的水。
第2步: 点燃燃烧匙内的红磷,并迅速伸入集气瓶中再塞紧塞子。
第3步: 待反应结束并冷却后,松开止水夹。此时水进入集气瓶,最终量筒中的水面停止在刻度V3毫升处。
请回答下列问题:
①在此设计方案中,红磷燃烧的化学方程式是______________________。
②实验中红磷必须要过量,目的是:_______________________。
③该方案中计算空气中氧气的体积分数的数学表达式为:______________。
【答案】锥形瓶 分液漏斗 2KMnO4![]() K2MnO4+ MnO2+O2↑ ADFG 防止加热时高锰酸钾粉末进入导管 b 4P+5O2
K2MnO4+ MnO2+O2↑ ADFG 防止加热时高锰酸钾粉末进入导管 b 4P+5O2![]() 2P2O5 耗尽集气瓶内氧气
2P2O5 耗尽集气瓶内氧气 ![]() ×100%
×100%
【解析】
(1)仪器B是锥形瓶,故填锥形瓶;仪器C是分液漏斗,故填分液漏斗;
(2)实验室用高锰酸钾制取氧气,反应生成了锰酸钾、二氧化锰和氧气,方程式故填2KMnO4![]() K2MnO4+ MnO2+O2↑;反应物是固体,反应条件是加热,选固体加热型发生装置,所以实验仪器选ADFG,故填ADFG;高锰酸钾制氧气时要在试管口塞一团棉花,防止加热时高锰酸钾粉末进入导管,故填防止加热时高锰酸钾粉末进入导管;
K2MnO4+ MnO2+O2↑;反应物是固体,反应条件是加热,选固体加热型发生装置,所以实验仪器选ADFG,故填ADFG;高锰酸钾制氧气时要在试管口塞一团棉花,防止加热时高锰酸钾粉末进入导管,故填防止加热时高锰酸钾粉末进入导管;
(3)用H装置收集氧气时,由于氧气密度比空气大,应该从b端进氧气,故填b;
(4)
①红磷燃烧生成五氧化二磷,方程式故填4P+5O2![]() 2P2O5;
2P2O5;
②实验时为了使实验结果更准确,要将集气瓶内氧气完全反应掉,红磷需要过量,故填耗尽集气瓶内氧气;
③在实验前后,量筒中水的体积变化就是燃烧消耗掉的集气瓶内氧气的体积,用氧气的体积除以集气瓶内空气的体积,在乘以百分之百就是空气中氧气的体积分数,故填![]() ×100%。
×100%。

【题目】在一定条件下,在一个密闭容器内发生某反应,测得反应过程中各物质的质量如表所示,下列说法不正确的是( )
物质 | X | Y | Z | W |
反应前质量/g | 10 | 3 | 90 | 0 |
反应后质量/g | 3.2 | 3 | 待测 | 3.2 |
A. W可能是单质 B. Y可能是催化剂
C. 该反应是分解反应 D. 反应后Z物质的质量为![]()