题目内容
请用“>”、“<”或“=”在下列横线上填空.
(1)浓盐酸的质量为A,敞口放置一段时间后,称得其质量为B,则A______B;
(2)质量为A的锌片插入硫酸铜溶液中,一段时间后取出附铜的锌片,干燥称得其质量为B,则A______B;
(3)20℃时,饱和硫酸铜溶液的溶质质量分数为A%,加入少量无水硫酸铜粉末,析出晶体后,该溶液的溶质质量分数为B%,则A______B.
解:(1)因浓盐酸易挥发,则浓盐酸溶液中溶质的质量减少,溶液的质量减小,即A>B,故答案为:>;
(2)因锌与硫酸铜的反应生成硫酸锌和铜,溶质由硫酸铜变为硫酸锌时,溶液质量会增加,则固体质量就减少,即A>B,故答案为:>;
(3)因温度不变,原溶液为饱和溶液,当加入少量无水硫酸铜粉末,析出晶体后,溶液仍然是该温度下的饱和溶液,由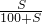 ×100%来质量分数,而溶解度S不变,则质量分数就不发生变化,即A%=B%,故答案为:=.
×100%来质量分数,而溶解度S不变,则质量分数就不发生变化,即A%=B%,故答案为:=.
分析:(1)根据浓盐酸易挥发来分析溶液的质量的变化;
(2)根据溶液中溶质的变化来分析固体的质量的变化;
(3)根据一定温度下饱和溶液中的溶解度来分析解答.
点评:本题考查知识点较多,主要考查物质的性质、金属与盐溶液的反应、饱和溶液中溶质质量分数的计算,学生应学会利用物质的特性及质量差等来分析溶液质量的变化,学会利用溶解度来计算饱和溶液中的溶质的质量分数.
(2)因锌与硫酸铜的反应生成硫酸锌和铜,溶质由硫酸铜变为硫酸锌时,溶液质量会增加,则固体质量就减少,即A>B,故答案为:>;
(3)因温度不变,原溶液为饱和溶液,当加入少量无水硫酸铜粉末,析出晶体后,溶液仍然是该温度下的饱和溶液,由
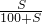 ×100%来质量分数,而溶解度S不变,则质量分数就不发生变化,即A%=B%,故答案为:=.
×100%来质量分数,而溶解度S不变,则质量分数就不发生变化,即A%=B%,故答案为:=.分析:(1)根据浓盐酸易挥发来分析溶液的质量的变化;
(2)根据溶液中溶质的变化来分析固体的质量的变化;
(3)根据一定温度下饱和溶液中的溶解度来分析解答.
点评:本题考查知识点较多,主要考查物质的性质、金属与盐溶液的反应、饱和溶液中溶质质量分数的计算,学生应学会利用物质的特性及质量差等来分析溶液质量的变化,学会利用溶解度来计算饱和溶液中的溶质的质量分数.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目


 (1)请用数字和化学符号表示下列物质或微粒:2个镁原子
(1)请用数字和化学符号表示下列物质或微粒:2个镁原子 下图表示物质分类和转化关系,请用物质类别、变化类型(“物理变化”或“化学变化”)和具体物质序号填空.(注意:示例选择从以下A、B、C、D四种物质中选择,把所有属于该类的选上.)
下图表示物质分类和转化关系,请用物质类别、变化类型(“物理变化”或“化学变化”)和具体物质序号填空.(注意:示例选择从以下A、B、C、D四种物质中选择,把所有属于该类的选上.)