题目内容
【题目】M元素的一种微粒的结构示意图为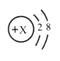 已知:
已知:
(1)M元素的单质是空气的重要组成部分,约占空气总体积的1/5,则x=_____。
(2)M元素与下列选项中_____(填序号)元素不能形成化合物。写出M元素组成的单质与下列元素组成的单质反应的化学方程式(任意一个)_____。
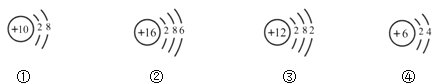
【答案】8 ① S+O2![]() SO2;2Mg+O2
SO2;2Mg+O2![]() 2MgO C+O2
2MgO C+O2![]() CO2.(任意一个)
CO2.(任意一个)
【解析】
(1)M元素的单质是空气的重要组成部分,约占空气总体积的1/5,则M元素是氧元素,氧元素的核内质子数8,故x=8;
(2)①表示的是原子,且最外层电子数=8,在化学反应中不易得失电子,化学性质稳定,与其它元素不能形成化合物;②核内质子数为16,是硫元素,硫和氧气在点燃条件下生成二氧化硫,反应方程式为:S+O2![]() SO2;③核内质子数为12,是镁元素,镁和氧气在点燃条件下生成氧化镁,反应方程式为:2Mg+O2
SO2;③核内质子数为12,是镁元素,镁和氧气在点燃条件下生成氧化镁,反应方程式为:2Mg+O2![]() 2MgO;④核内质子数为6,是碳元素,碳和氧气在点燃条件下生成二氧化碳,反应方程式为:C+O2
2MgO;④核内质子数为6,是碳元素,碳和氧气在点燃条件下生成二氧化碳,反应方程式为:C+O2 ![]() CO2。
CO2。

 阅读快车系列答案
阅读快车系列答案【题目】在工业中硫酸铜有不少用途。某工厂用硫化铜(CuS)制硫酸铜,拟选择两个方案。
方案 | 方案① | 方案② |
原理 | CuS是在硫杆菌(催化剂)的作用下与空气中的氧气发生化合反应生成硫酸铜 | 2CuS+3O2 CuO+H2SO4=CuSO4+H2O |
(1)请写出方案①反应的化学方程式_____。
(2)在两个方案中①更合理。理由是方案①具有以下优点:
优点一:_____优点二:_____。
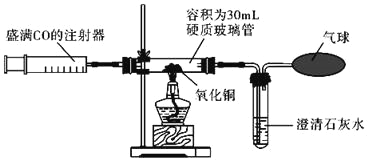
【题目】据报道,我国超市每年消耗约40万吨塑料袋。其中聚乙烯塑料袋无毒,可以包装食品,其组成中只含C、H元素,若把废聚乙烯塑料袋通过焚烧处理,将会排放大量CO2气体。某兴趣小组欲测量一定质量聚乙烯塑料袋燃烧后产生CO2的质量,设计了以下实验装置,装置A中小烧杯里加入的是H2O2和MnO2,装置B里加入的是浓硫酸,装置C里加入的是碱石灰。
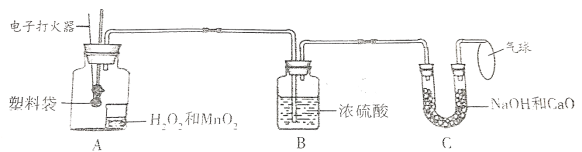
(查阅资料)NaOH和CaO的混合物俗称碱石灰,碱石灰能吸收水分和二氧化碳。
(实验探究)
实验步骤 | 实验现象 | 实验结论或化学方程式 |
①把H2O2倒入盛有少量MnO2小烧杯里有的小烧杯里,观察现象 | 小烧杯里有_____ | 反应的化学方程式为_____ |
②用电子打火器点燃缠绕在玻璃棒上的废聚乙烯塑料袋,观察废聚乙烯塑料袋现象 | 废聚乙烯塑料袋_____ | 装置B中浓硫酸的质量_____ 装置C中碱石灰的质量_____ |
(评价反思)
(1)装置A小烧杯中加入H2O2和MnO2的目的是_____
(2)装置B中浓硫酸的作用是_____
(3)装置C中碱石灰的作用是_____
(4)根据实验目的,需要进行称量的是_____
①实验前塑料袋的质量
②实验前和实验后装置B的质量
③实验前和实验后装置C的质量