题目内容
实验室有一瓶试剂,密封完好但标签残缺,只剩下“Na”和“10%”字样.已知它是无色液体,是初中化学常用的试剂.小丰和小安同学很感兴趣,决定对其成分进行探究.
提出问题:这瓶试剂可能是什么溶液呢?
交流讨论:根据受损标签的情况判断,这瓶试剂不可能是
A、酸 B、碱 C、盐
查阅资料:
I、初中化学常见的含钠化合物有NaCl、NaOH、
II、Na2CO3和NaHCO3溶液呈碱性:
III、室温(20°C)时,四种物质的溶解度的数据如下:
| 物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
| 溶解度g | 36 | 109 | 215 | 9.6 |
得出结论:小安根据试剂瓶标注的溶质质量分数10%和上表中的溶解度的数据判断,这瓶试剂不可能是 .
设计实验并继续探究:
(1)小丰用洁净的玻璃棒蘸取该溶液滴在PH试纸上,测得PH>7,这瓶试剂不可能是 .
(2)小丰为了确定该溶液是哪种溶液,他又进行了如下实验:
| 操作步骤 | 实验现象 | 结论及化学方程式 |
| 取样于试管中,滴 加 | 产生大量的气泡 | 该溶液是 ,反应的化学方程式 |
小丰为了探究一瓶CaCl2溶液的质量分数,取该溶液50g,加入50gNa2CO3溶液,恰好完全反应,所得溶液质量95g,请你计算所用CaCl2溶液的质量分数?
【交流讨论】A;【得出结论】NaHCO3;【设计实验并继续探究】(1)NaCl
(2)操作步骤实验现象结论及化学方程式
稀盐酸(或稀硫酸)碳酸钠溶液
Na2CO3+2HCl═2NaCl+H2O+CO2↑
所用CaCl2溶液的质量分数11.1%.
解析试题分析:【交流讨论】酸当中不可能含有钠离子,故该溶液不可能是酸,故本题答案为:A;【得出结论】根据计算可以知道在20℃时饱和碳酸氢钠的质量分数为: ×100%=8.8%<10%,所以能够排除碳酸氢钠,故本题答案为:NaHCO3;【设计实验并继续探究】(1)小强用洁净的玻璃棒蘸取该溶液滴在pH试纸上,测得pH>7,而氯化钠溶液呈中性,pH等于7所以不可能是氯化钠,故本题答案为:NaCl(2)小强为了检验该溶液是NaOH溶液还是Na2CO3溶液,他又进行了如下实验:根据碳酸钠可以和盐酸反应可以设计实验来验证碳酸钠的存在,如果产生气泡,则说明是碳酸钠,反之为氢氧化钠,故本题答案为:
×100%=8.8%<10%,所以能够排除碳酸氢钠,故本题答案为:NaHCO3;【设计实验并继续探究】(1)小强用洁净的玻璃棒蘸取该溶液滴在pH试纸上,测得pH>7,而氯化钠溶液呈中性,pH等于7所以不可能是氯化钠,故本题答案为:NaCl(2)小强为了检验该溶液是NaOH溶液还是Na2CO3溶液,他又进行了如下实验:根据碳酸钠可以和盐酸反应可以设计实验来验证碳酸钠的存在,如果产生气泡,则说明是碳酸钠,反之为氢氧化钠,故本题答案为:
操作步骤实验现象结论及化学方程式
稀盐酸(或稀硫酸)碳酸钠溶液
Na2CO3+2HCl═2NaCl+H2O+CO2↑
设原溶液中CaCl2的质量为x,
根据质量守恒定律,产生碳酸钙的质量为:50g+50g﹣95g=5g
CaCl2+K2CO3═CaCO3↓+2KCl
111 100
x 5g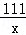 =
=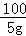
x=5.55g
则溶液中中CaCl2的质量分数为: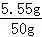 ×100%=11.1%
×100%=11.1%
答:所用CaCl2溶液的质量分数11.1%.
考点:缺失标签的药品成分的探究;有关溶质质量分数的简单计算;根据化学反应方程式的计算.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案某化学学习小组的同学围绕“澄清石灰水与碳酸钠溶液的反应”展开了如下探究活动。(1)该反应的化学方程式为________________________________。
(2)反应后溶液中的溶质是什么?同学们一致认为有以下三种情况:
①氢氧化钠和氢氧化钙;②氢氧化钠和碳酸钠;③_______________。
(3)小新取少量溶液于试管中,滴加过量稀盐酸,发现无气泡产生,说明情况_____(填序号)是不可能的。
为了进一步确定溶液的成分,同学们设计了如下实验方案:
| 实验步骤 | 现象 | 结论 |
| | | 情况①正确 |
在同学们的合作下,他们顺利完成了探究任务。
某化学兴趣小组在化学实验室发现一瓶没有标签的淡黄色粉末,同学们对探究该粉末产生浓厚兴趣,并在老师的指导下进行探究活动。
【提出问题】这种淡黄色粉末是什么?有什么性质和用途?
【查阅资料】①硫是淡黄色粉末,不溶于水;
②过氧化钠(Na2O2)是淡黄色粉末,溶于水并能与水反应,“载人宇宙飞船或潜水艇中一般都要安装盛放过氧化钠(Na2O2)颗粒的装置”
【猜想与探究】
猜想:淡黄色粉末可能是:a.硫;b.过氧化钠;c.硫和过氧化钠的混合物
【实验与结论】
| | 实验操作 | 实验现象 | 实验结论 |
| 猜想 | 在一支洁净的试管中加入适量的上述淡黄色粉末,再加入足量的蒸馏水,充分振荡 | | 猜想a、c不成立,猜想b成立。 |
【提出问题】过氧化钠是否为一种制氧剂?与人呼出的哪种气体发生反应?
【提出猜想】过氧化钠与人呼出的N2或CO2或水蒸气反应并生成氧气。
【进行实验】
实验Ⅰ:验证过氧化钠与氮气反应并生成氧气。

王轩同学设计如下图所示装置:
(1)实验现象及结论:观察到____________现象,判断过氧化钠与氮气没有发生反应。
实验Ⅱ:验证过氧化钠与水蒸气反应并生成氧气。
华宇同学设计了如下图所示装置
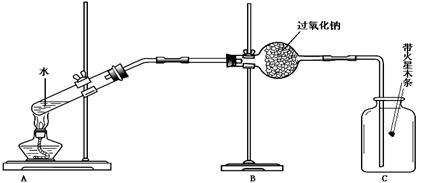
(2)其中A装置的作用是____________。
(3)实验现象及结论:带火星的木条复燃。
实验Ⅲ:验证过氧化钠与二氧化碳反应并生成氧气。李杰在老师的指导下也设计了如下图所示装置。(不考虑稀盐酸的挥发)
| 实验操作 | 主要实验现象 | 实验结论及解释 | |
| ① | 检查装置的气密性。 向装置中加入药品。 | | 装置的气密性良好。 |
| ② | 打开分液漏斗活塞,向A装置中缓慢加入稀盐酸。 | A装置中观察到的现象有__________, C装置中有气泡出现。 | A装置中发生反应的化学方程式为________; (2分) |
| ③ | 一段时间后用带火星的木条在D内进行检验。 | 带火星的木条复燃。 | 过氧化钠与二氧化碳反应并生成氧气。 |

(4)实验记录
【实验反思】
张红同学对实验Ⅲ的设计提出疑问:该实验不能证明二氧化碳与过氧化钠确实发生了反应,你认为他的理由是_____ ___。请你回答如何改进该实验 。







