题目内容
(3分)金属单质A与非金属单质硫(S)发生如下反应: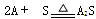 。甲、乙、丙三组学生在实验室分别进行该实验,加入的A和硫的质量各不相同,但总质量均为6 g。充分反应时,实验数据记录如下:
。甲、乙、丙三组学生在实验室分别进行该实验,加入的A和硫的质量各不相同,但总质量均为6 g。充分反应时,实验数据记录如下:
| | A的质量/ g | S的质量/ g | A2S的质量/ g |
| 甲 | 5 | 1 | 5 |
| 乙 | 4 | 2 | 5 |
| 丙 | a | b | 3 |
(1)元素A的相对原子质量为 。
(2)丙组实验中a∶b为 (结果以最简整数比表示,请写出计算过程)。
(1)64 (2)a∶b为2∶3或9∶1
解析试题分析:对比甲、乙两同学所用A和S的质量及生成A2S的质量:同样生成5gA2S,甲实验中S的用量为1g、乙实验中S的用量为2g,则说明反应生成5g的A2S时,需要消耗S的质量为1g;利用质量守恒定律,可判断生成5g的A2B时,消耗A的质量为4g,即两物质恰好完全反应时,A、S两物质的用量比为4:1。
(1)设元素A的相对原子质量是x
2A + S═A2S
2x 32
4g 1g
2x:32 =4g:1g
解得,x=64
(2)由于丙同学实验中生成A2S的质量为3g,而反应中反应物A、S两物质的质量比为4:1,则参加反应的A的质量=3g×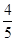 =2.4g,参加反应的S的质量=3g-2.4g=0.6g,则剩余物的质量为3g;若A剩余,则a∶b=(2.4g+3g):0.6g=9:1;若S剩余,则a∶b=2.4g:(0.6g+3g)=2:3。
=2.4g,参加反应的S的质量=3g-2.4g=0.6g,则剩余物的质量为3g;若A剩余,则a∶b=(2.4g+3g):0.6g=9:1;若S剩余,则a∶b=2.4g:(0.6g+3g)=2:3。
考点:根据化学反应方程式的计算
点评:本题主要考查学生利用物质之间的质量比,计算未知的物质的质量的能力,解题的关键是根据已知条件求出物质之间的质量比,要注意全面考虑可能存在的情况。

金属单质A与非金属单质硫(S)发生如下反应: A + S  AS。甲、乙、丙三组学生在实验室分别进行该实验,加入的A和硫的质量各不相同,但总质量均为12g。
分别反应时,实验数据记录如下:
AS。甲、乙、丙三组学生在实验室分别进行该实验,加入的A和硫的质量各不相同,但总质量均为12g。
分别反应时,实验数据记录如下:
|
|
A的质量/ g |
S的质量/ g |
AS的质量/ g |
|
甲 |
8 |
4 |
11 |
|
乙 |
7 |
5 |
11 |
|
丙 |
a |
b |
6.6 |
根据上述信息,计算(请写出计算过程):
(1)元素A的相对原子质量。
(2)丙组实验中a∶b为 (结果以最简整数比表示)。
(3分)金属单质A与非金属单质硫(S)发生如下反应: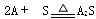 。甲、乙、丙三组学生在实验室分别进行该实验,加入的A和硫的质量各不相同,但总质量均为6 g。充分反应时,实验数据记录如下:
。甲、乙、丙三组学生在实验室分别进行该实验,加入的A和硫的质量各不相同,但总质量均为6 g。充分反应时,实验数据记录如下:
|
|
A的质量/ g |
S的质量/ g |
A2S的质量/ g |
|
甲 |
5 |
1 |
5 |
|
乙 |
4 |
2 |
5 |
|
丙 |
a |
b |
3 |
根据上述信息,回答问题:
(1)元素A的相对原子质量为 。
(2)丙组实验中a∶b为 (结果以最简整数比表示,请写出计算过程)。