题目内容
【题目】金属材料在生产、生活中广泛应用,有许多性质等内容需要探究。
(1)下表提供了在一定条件下,水能否与一些金属发生反应的信息。
①请根据金属活动性顺序和表中的已知信息,将表格填写完整。
物质 | 钠与冷水 | 镁与冷水 | 镁与水蒸汽 | 铁与冷水 | 铁与水蒸气 |
能否发生反应 | 剧烈反应 | 缓慢反应 | 不反应 | 加热条件下能反应 |
②虽然铁在常温下与水不反应,但铁制品在潮湿的环境中很容易生锈。某同学进行了如右图所示实验。一周以后发现铁钉表面锈蚀。在右图中a、b、c三处,锈蚀情况最严重的是(填字母)。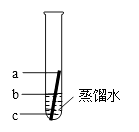
(2)镁条在空气中久置表面会变黑,某小组同学设计并进行实验,探究镁条变黑的条件。
【查阅资料】①常温下,亚硫酸钠(Na2SO3)可与O2发生化合反应;
②浓硫酸具有吸水性。
【猜想与假设】常温下,镁条变黑可能与O2、CO2、水蒸气有关。
【进行实验】通过控制与镁条接触的物质,利用如图装置(镁条长度为3cm,试管容积为20mL),分别进行下列5个实验, 并持续观察20天。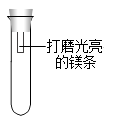
编号 | 主要实验操作 | 实验现象 |
① | 先充满用NaOH浓溶液洗涤过的空气; | 镁条始终无明显变化 |
② | 加入2mLNaOH浓溶液 | 镁条始终无明显变化 |
③ | 先加入2mL浓硫酸; | 镁条始终无明显变化 |
④ | 先加入4mL饱和Na2SO3溶液; | 镁条始终无明显变化 |
⑤ | 先加入2mL蒸馏水; | 镁条第3天开始变黑, |
【解释与结论】
①实验1和2中,NaOH浓溶液的作用是(用化学方程式表示)。
②实验1的目的是。
③实验3中,试管内的气体主要含有CO2、。
④得出“镁条变黑一定与CO2有关”的结论,依据的两个实验是(填编号)。
⑤由上述实验可推知,镁条变黑的条件是。
(3)【反思与评价】
⑥在猜想与假设时,同学们认为镁条变黑与N2无关,其理由是。
⑦欲进一步证明镁条表面的黑色物质中含有碳酸盐,所需试剂是。
【答案】
(1)剧烈反应,b
(2)NaOH+CO2=Na2CO3+H2O,检验只用O2是否会使镁条变黑,O2(N2可填写可不填写),2、5,H2O、CO2、O2
(3)常温下氮气的化学性质不活泼,很难和其他物质反应,稀盐酸和澄清石灰水
【解析】(1).根据表格可以发现,铁与冷水不反应,与水蒸气能反应,说明温度影响反应的进行,在金属活动性顺序中镁在铁的前面,活动性比铁强,故镁能与水蒸气反应, (2). 铁生锈是铁与氧气、水三种物质共同作用的结果,b处三种物质接触最充分,生锈最严重; (3). NaOH浓溶液的作用是是吸收二氧化碳,反应方程式为:2NaOH+CO2=Na2CO3+H2O (4). 实验1中用浓硫酸除掉了水,用氢氧化钠除掉了二氧化碳,所以目的是检验只用O2是否会使镁条变黑 (5). 实验3中,用浓硫酸除掉了水,试管内的气体主要含有CO2、O2, (6). 实验2中除掉了二氧化碳,镁条始终无明显变化;实验5中先加入2mL蒸馏水,再通入约4mLCO2,镁条第3天开始变黑,至20天全部变黑;因此得出“镁条变黑一定与CO2有关”的结论,依据的两个实验是. 2、5 (7). 由上述实验可推知,镁条变黑的条件是H2O、CO2、O2 (8). 镁条变黑与N2无关,其理由是常温下氮气的化学性质不活泼,很难和其他物质反应 (9). 欲进一步证明镁条表面的黑色物质中含有碳酸盐,所需试剂是稀盐酸和澄清石灰水,加入盐酸生成气体,将气体通入澄清石灰水中,澄清石灰水变浑浊。
【考点精析】认真审题,首先需要了解科学探究的基本环节(一般步骤:提出问题→猜想与假设→设计实验→实验验证→记录与结论→反思与评价).

【题目】将一定量的锌粉投入到硝酸银、硝酸铜的混合溶液中,充分反应后过滤,得到滤液和滤渣,若所得滤液呈无色,则滤液中一定含有的金属阳离子为_____(填离子符号),滤渣中一定含有的金属单质有_____。
【题目】青岛市2019年5月20曰的空气质日报如下:
项目 | 空气污指数 | 空气质量级别 | 空气质量 |
可吸入颗粒物 | 65 | II | 良 |
二氧化硫 | 6 | ||
二氧化氮 | 20 |
下列各项对表中三个空气质量指标不会产生影响的是( )
A. 露天焚饶垃圾B. 用煤做燃料
C. 用氢气做燃料D. 货车运输建筑垃圾沿途撒漏