题目内容
如图是某学生绘制的元素周期表的一部分:
请根据相关信息与知识回答:
(1)1869年,俄国化学家
(2)氦、氖、氩等稀有气体的化学性质很不活泼,其原因是
(3)请写出原子序数分别为8、13两种元素组成的化合物的化学式
| 1 H 氢 |
2He 氦 | ||||||
| 3 Li 锂 |
4 Be 铍 |
5 B 硼 |
6 C 碳 |
7 N 氮 |
8O 氧 |
9F 氟 |
10Ne 氖 |
| 11 Na 钠 |
12 Mg 镁 |
13 Al 铝 |
14 Si 硅 |
15 P 磷 |
16S 硫 |
17Cl 氯 |
18Ar 氩 |
(1)1869年,俄国化学家
门捷列夫
门捷列夫
发现了元素周期律并编制了元素周期表;(2)氦、氖、氩等稀有气体的化学性质很不活泼,其原因是
它们原子的最外层电子数均已达到稳定结构
它们原子的最外层电子数均已达到稳定结构
;(3)请写出原子序数分别为8、13两种元素组成的化合物的化学式
Al2O3
Al2O3
.分析:(1)根据化学家的贡献判断;
(2)根据最外层电子数决定了元素的化学性质分析;
(3)根据化合价书写化学式的方法;
(2)根据最外层电子数决定了元素的化学性质分析;
(3)根据化合价书写化学式的方法;
解答:解:(1)门捷列夫发现元素周期律并编制出元素周期表;
(2)最外层电子数决定了元素的化学性质,氦、氖、氩等稀有气体的化学性质很不活泼是因为它们原子的最外层电子数均为8,是稳定结构,故答案为:(3)原子序数分别为8是氧元素,化合价为-2价,原子序数分别为13是铝元素,化合价为+3价,所以氧化铝的化学式为Al2O3;
故答案为:门捷列夫;它们原子的最外层电子数均已达到稳定结构;Al2O3;
(2)最外层电子数决定了元素的化学性质,氦、氖、氩等稀有气体的化学性质很不活泼是因为它们原子的最外层电子数均为8,是稳定结构,故答案为:(3)原子序数分别为8是氧元素,化合价为-2价,原子序数分别为13是铝元素,化合价为+3价,所以氧化铝的化学式为Al2O3;
故答案为:门捷列夫;它们原子的最外层电子数均已达到稳定结构;Al2O3;
点评:本题考查学生根据元素周期表的具体应用知识,涉及到最外层电子数相同的元素化学性质相似并将元素周期律灵活应用的能力.

练习册系列答案
相关题目
 如图是某学生绘制的元素周期表的一部分:
如图是某学生绘制的元素周期表的一部分: (2012?攀枝花)如图是某学生绘制的元素周期表的一部分:
(2012?攀枝花)如图是某学生绘制的元素周期表的一部分: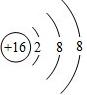 ,该离子的符号为
,该离子的符号为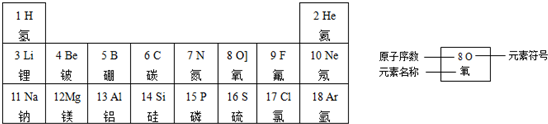
 ,该元素离子的符号为
,该元素离子的符号为