题目内容
某实验小组的同学用氢氧化钙溶液和盐酸进行酸碱中和反应的实验时,向烧杯中的氢氧化钙溶液加入一定量稀盐酸后,发现忘记了滴加指示剂.因此,他们停止滴加稀盐酸,并对烧杯内溶液中的溶质成分进行探究.
Ⅰ.探究烧杯内溶液中溶质的成分.
【提出问题】该烧杯内溶液中的溶质是什么?
【猜想】猜想一:Ca(OH)2和HCl; 猜想二:CaCl2和Ca(OH)2;
猜想三: ______ ; 猜想四:CaCl2和HCl.
根据所学知识判断,猜想一一定不成立,理由一是 ______ ;理由二是 ______ .
【查阅资料】氯化钙溶液呈中性,碳酸钠溶液呈碱性.
【进行实验】
实验步骤:取少量烧杯内溶液于试管中,滴入几滴酚酞溶液,振荡.
实验现象: ______ .
结论:猜想二不成立
实验步骤:取少量烧杯内溶液于另一支试管中,逐滴加入碳酸钠溶液至过量.
实验现象: ______ .
结论:猜想三不成立,猜想四成立
【反思与拓展】
(1)在分析化学反应后所得物质成分时,除考虑生成物外还需考虑 ______ .
(2)烧杯中的溶液未经处理直接倒入下水道,可能造成的危害是 ______ (写一条即可).要处理烧杯内的溶液,使其溶质只含有CaCl2,应向烧杯中加入过量的 ______ .
化学兴趣课上,同学们对过氧化钠(Na2O2)可以做供氧剂产生了浓厚兴趣,于是在老师的指导下展开了以下探究活动。
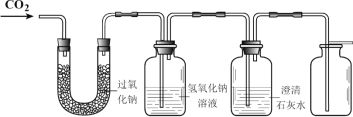
(提供资料)① 二氧化碳与过氧化钠反应生成氧气和另一种物质。② 碳酸钠(Na2CO3)、碳酸氢钠(NaHCO3)与盐酸反应均能生成CO2。③ 2Na2O2 + 2H2O === 4NaOH + O2↑。
(1)证明二氧化碳与过氧化钠反应产生氧气并收集一瓶氧气。
同学们在老师的指导下设计了如上图所示装置。
① 如何证明氧气已经收集满______。
② 氢氧化钠溶液的作用是除去未反应的二氧化碳,若观察到______,说明二氧化碳已经除尽。
(2)探究二氧化碳与过氧化钠反应生成的另一种物质。
(猜想与假设)下面是同学们提出的3种猜想。
猜想1:是氢氧化钠 猜想2:是碳酸氢钠 猜想3:是碳酸钠
通过对反应物中有关元素的组成分析,你认为猜想______是不正确的,理由是______。
(进行实验)同学们通过以下实验验证了另一种物质,请完成下述实验报告。
实验操作 | 实验现象 | 实验结论 |
取少量CO2与Na2O2反应后的固体于试管中,______。 | 有大量气泡产生,澄清石灰水变浑浊。 | 猜想______是正确的。 |
澄清石灰水变浑浊的化学方程式为______
(反思与评价)若用人呼出的气体通过上图装置,证明二氧化碳与过氧化钠反应生成了氧气,你是否同意这种做法,并阐述理由_______________。