题目内容
现有10%的氯化钠溶液50g,若使其溶质质量分数增达到20%,可采用的方法是:①需要蒸发多少克水?②需要加入多少g 氯化钠?
【答案】分析:若使质量分数为10%的氯化钠溶液变成20%的溶液,可采取加入溶质氯化钠继续溶解或蒸发部分溶剂水的方法;增加溶质时,溶剂质量不变,溶液质量随溶质溶解而增加;蒸发溶剂时,溶质质量不变而溶剂减少溶液质量也随之减小;根据溶质质量分数=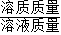 ×100%计算变化中增加溶质的质量或蒸发溶剂的质量即可.
×100%计算变化中增加溶质的质量或蒸发溶剂的质量即可.
解答:解:①若蒸发溶剂使溶质的质量分数变大,设蒸发水的质量为xx,
根据蒸发前后溶质的质量不变,得
50g×10%=(50g-x)×20%
解得:x=25g,
即蒸发25g水可使氯化钠溶液的溶质的质量分数达到20%;
②若增加溶质,设增加的溶质的质量为y,
根据混合前的溶质质量等于混合后溶液中的溶质质量,得
50g×10%+y=(50g+y)×20%,
解得:y=6.25g,
即增加6.25g氯化钠溶质可使溶质的质量分数达到20%;
答:①需要蒸发25g水
②需要加入6.25g 氯化钠
点评:在不析出晶体时蒸发溶剂水可使溶液的溶质质量分数因溶剂的减小而增大;在未达到饱和状态时加入溶解继续溶解,可使溶液的溶质质量分数因溶质质量的增加而增大.
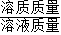 ×100%计算变化中增加溶质的质量或蒸发溶剂的质量即可.
×100%计算变化中增加溶质的质量或蒸发溶剂的质量即可.解答:解:①若蒸发溶剂使溶质的质量分数变大,设蒸发水的质量为xx,
根据蒸发前后溶质的质量不变,得
50g×10%=(50g-x)×20%
解得:x=25g,
即蒸发25g水可使氯化钠溶液的溶质的质量分数达到20%;
②若增加溶质,设增加的溶质的质量为y,
根据混合前的溶质质量等于混合后溶液中的溶质质量,得
50g×10%+y=(50g+y)×20%,
解得:y=6.25g,
即增加6.25g氯化钠溶质可使溶质的质量分数达到20%;
答:①需要蒸发25g水
②需要加入6.25g 氯化钠
点评:在不析出晶体时蒸发溶剂水可使溶液的溶质质量分数因溶剂的减小而增大;在未达到饱和状态时加入溶解继续溶解,可使溶液的溶质质量分数因溶质质量的增加而增大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目