题目内容
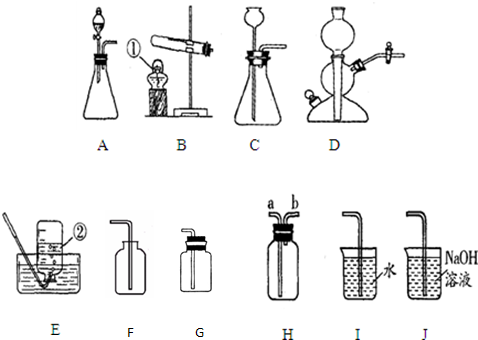
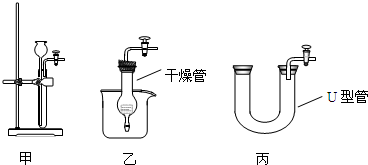
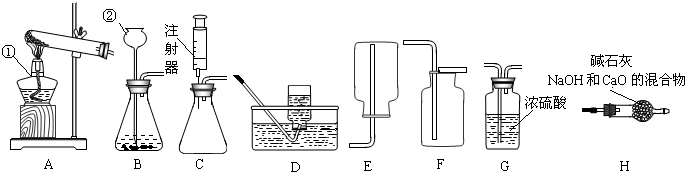
某研究性学习小组欲利用下列装置进行相关气体制取的探究,请你分析并填空.

(1)图中仪器a的名称为______;
(2)实验室制取二氧化碳的化学方程式是______,应选择的气体发生装置是和收集装置是______.
(3)实验室加热氯酸钾和二氧化锰制取氧气的化学方程式是______,应选择的发生装置是______,若用盛满水的F装置收集氧气,应从导管______(填①或②)通入.
(4)甲烷是一种无色、无味、难溶于水的气体,实验室用加热无水醋酸钠和碱石灰的固体混合物的方法制取甲烷,则实验室制取并收集甲烷应选择的装置组合是______.
(5)在科学家眼里,二氧化碳是可以利用的重要资源.在一定条件下,二氧化碳和金属钠反应可以制金刚石[CO2+4Na C(金刚石)+2Na2O],请计算92g金属钠理论上可制得含碳96%的金刚石的质量.
C(金刚石)+2Na2O],请计算92g金属钠理论上可制得含碳96%的金刚石的质量.
解:(1)图中仪器a是试管;
(2)实验室用大理石和盐酸反应生成氯化钙、水和二氧化碳,方程式是:CaCO3+2HCl=CaCl2+H2O+CO2↑;该反应不需加热,属于固液常温型,故选发生装置B,二氧化碳的密度比空气大且能溶于水,所以用向上排空气法收集;
(3)氯酸钾在加热和二氧化锰作催化剂的条件下生成氯化钾和氧气,方程式是2KClO3 2KCl+3O2↑,该反应需要加热,属于固体加热型,故选发生装置A;若用盛满水的F装置收集氧气,应从导管②进气,将水挤压到集气瓶底部,从长导管排出;
2KCl+3O2↑,该反应需要加热,属于固体加热型,故选发生装置A;若用盛满水的F装置收集氧气,应从导管②进气,将水挤压到集气瓶底部,从长导管排出;
(4)用加热无水醋酸钠和碱石灰的固体混合物的方法制取甲烷,属于固体加热型,故选发生装置A,甲烷难溶于水,其密度比空气小(相对分子质量=16<29),所以可用排水法或向下排空气法收集;
(5)设92g金属钠理论上可制得含碳96%的金刚石的质量为x
CO2+4Na C(金刚石)+2Na2O
C(金刚石)+2Na2O
92 12
92g 96%?x
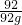 =
=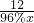
x=12.5g
答:92g金属钠理论上可制得含碳96%的金刚石的质量为12.5g.
故答案为:
(1)试管;
(2)CaCO3+2HCl=CaCl2+H2O+CO2↑; B和D;
(3)2KClO3 2KCl+3O2↑; A; ②;
2KCl+3O2↑; A; ②;
(4)AC或AE;
(5)12.5g.
分析:(1)据常用仪器回答;
(2)据实验室制取二氧化碳的反应原理书写方程式,并据反应物状态和反应条件选择发生装置,据二氧化碳的密度和溶解性选择收集装置;
(3)氯酸钾在加热和二氧化锰作催化剂的条件下生成氯化钾和氧气,据此书写方程式,并选择发生装置,排水法收集气体分析解答;
(4)据发生和收集装置的选取方法分析解答;
(5)根据二氧化碳和金属钠的反应,结合题给的金属钠的质量可以求算出能够制得的金刚石的质量.
点评:要想解答好这类题目,首先要掌握发生和收集装置的选取方法、反应原理,理解和熟记根据化学反应方程式的计算步骤和格式,以及与之相关的知识等.然后,根据所给的问题情景或图表信息等,结合所学的相关知识和技能,按照题目要求认真分析解答即可.
(2)实验室用大理石和盐酸反应生成氯化钙、水和二氧化碳,方程式是:CaCO3+2HCl=CaCl2+H2O+CO2↑;该反应不需加热,属于固液常温型,故选发生装置B,二氧化碳的密度比空气大且能溶于水,所以用向上排空气法收集;
(3)氯酸钾在加热和二氧化锰作催化剂的条件下生成氯化钾和氧气,方程式是2KClO3
 2KCl+3O2↑,该反应需要加热,属于固体加热型,故选发生装置A;若用盛满水的F装置收集氧气,应从导管②进气,将水挤压到集气瓶底部,从长导管排出;
2KCl+3O2↑,该反应需要加热,属于固体加热型,故选发生装置A;若用盛满水的F装置收集氧气,应从导管②进气,将水挤压到集气瓶底部,从长导管排出;(4)用加热无水醋酸钠和碱石灰的固体混合物的方法制取甲烷,属于固体加热型,故选发生装置A,甲烷难溶于水,其密度比空气小(相对分子质量=16<29),所以可用排水法或向下排空气法收集;
(5)设92g金属钠理论上可制得含碳96%的金刚石的质量为x
CO2+4Na
 C(金刚石)+2Na2O
C(金刚石)+2Na2O92 12
92g 96%?x
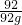 =
=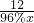
x=12.5g
答:92g金属钠理论上可制得含碳96%的金刚石的质量为12.5g.
故答案为:
(1)试管;
(2)CaCO3+2HCl=CaCl2+H2O+CO2↑; B和D;
(3)2KClO3
 2KCl+3O2↑; A; ②;
2KCl+3O2↑; A; ②;(4)AC或AE;
(5)12.5g.
分析:(1)据常用仪器回答;
(2)据实验室制取二氧化碳的反应原理书写方程式,并据反应物状态和反应条件选择发生装置,据二氧化碳的密度和溶解性选择收集装置;
(3)氯酸钾在加热和二氧化锰作催化剂的条件下生成氯化钾和氧气,据此书写方程式,并选择发生装置,排水法收集气体分析解答;
(4)据发生和收集装置的选取方法分析解答;
(5)根据二氧化碳和金属钠的反应,结合题给的金属钠的质量可以求算出能够制得的金刚石的质量.
点评:要想解答好这类题目,首先要掌握发生和收集装置的选取方法、反应原理,理解和熟记根据化学反应方程式的计算步骤和格式,以及与之相关的知识等.然后,根据所给的问题情景或图表信息等,结合所学的相关知识和技能,按照题目要求认真分析解答即可.

练习册系列答案
相关题目
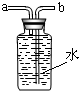 收集乙炔,气体应从
收集乙炔,气体应从