题目内容
液晶是一种新型材料,其化学式是C18H21NO.从这个化学式中得出的结论正确的是( )
A. 该材料由C、H、O三种元素组成
B. 该材料中氢元素的质量分数最小
C. 该材料中一共有41个原子
D. C18H21NO的相对分子质量为267
 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案生活中蕴含着许多化学知识与原理.
(1)铝塑板是一种房屋装修材料,它是在聚乙烯塑料中加入氢氧化铝等物质而制成.聚乙烯塑料属于_____(填标号).
A 金属材料 B 无机非金属材料 C 合成材料
(2)使用洗洁精更容易洗去餐具上的油污,其中蕴含的化学原理是:_____(选填“溶解”、“乳化”或“催化”)作用.
(3)在抗击旱灾的过程中,需要用到大量的干冰.干冰主要是用于:_____.
(4)下表是几种植物生长最适宜的pH范围.某地土壤呈弱碱性,你认为该地最适宜种植的作物是_____.
农作物 | 茶树 | 烟草 | 水稻 | 甘草 |
pH | 5.0~5.5 | 5.0~6.0 | 6.0~7.0 | 7.2~8.5 |
(5)一种“即食即热型快餐”适合外出旅行时使用.其原理是利用镁粉与水反应放出的热对食物进行加热.镁与水反应生成氢氧化镁和氢气的化学方程式是_____,反应中放出的热能是由_____能转化成的.
实验室有一包固体药品,可能含有BaSO4、Na2CO3、CuSO4、NaCl、CaCl2、NaOH中的一种或几种,为确定其成分,某班同学在老师的指导下进行探究。
[定性探究]
(1)称取少量样品,加入足量水中充分溶解,过滤后得到白色沉淀和无色滤液。由实验现象可知,原固体中一定不含_____。
(2)取(1)中得到的滤液少量,设计实验继续探究原固体的成分,请帮他们完成实验报告并回答问题。
操作 | 现象 | 结论 |
①向滤液中加入足量氯化钙溶液 | 产生白色沉淀 | 原固体中一定含有_____ |
②取①中上层清液,滴加_____ | _____ | 原固体中不含NaOH |
其中,步骤①加入足量氯化钙溶液的目的除了检验一定含有的物质外,还能起到的作用是_____。
(3)再取(1)中得到的滤液少量,进行如图1所示操作:
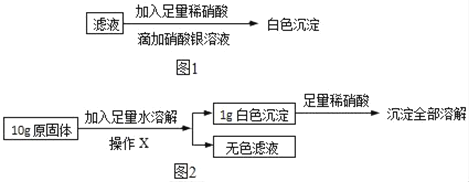
同学们认为:原固体中一定含有NaCl.但是老师指出这个结论不正确,其理由是_____(填序号)。
A 滤液中含有Na2CO3,也能和AgNO3反应生成沉淀
B 滤液中的NaCl可能是由原固体中的Na2CO3和CaCl2反应生成
[定量探究]
(4)在老师的指导下同学们又精确称量了10g原固体,进行如图2实验:
同学们认为,根据“沉淀全部溶解”的现象可确定白色沉淀的成分是_____,则原固体中一定不含_____;其中,操作X的名称是_____,无色滤液中一定含有的阳离子是_____。根据生成沉淀的质量计算原固体中氯化钙的质量分数是_____。