题目内容
【题目】HQ中学化学兴趣小组同学用四种方法区分氯化钡和氢氧化钡溶液。
(提出问题)如何用四种方法区分氯化钡溶液和氢氧化钡溶液?
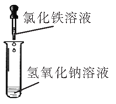
(实验设计)取8支试管分为以下四组为:A组、B组、C组、D组,每组两支试管①②;A组试管中分别滴加酚酞溶液;B组试管中分别滴加氯化铁溶液;C组试管中通入二氧化碳气体;D组试管滴加稀硫酸。
分组如图:
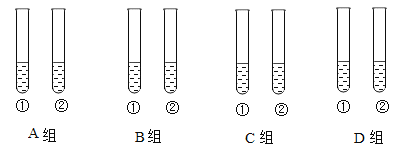
通过上述实验观察和分析,回答下列问题:
(1)(实验观察与分析)若在C组的①试管中观察到溶液中产生白色沉淀这一明显实验现象,则可确定B组中①试管内发生反应的方程式:________;
(2)(实验探究1)实验结束后,小组同学将A组与D组的废液倒入同一个废液缸中混合后过滤,得到无色滤液,在过滤操作中需要的用品除了带铁圈的铁架台以外还需要________,然后对所得滤液中离子的组成进行探究。
(3)(猜想与假设)猜想1:Cl-、H+
猜想2:Cl-、Ba2+
猜想3:Cl-、H+、SO42-
猜想4:Cl-、H+、Ba2+;
(设计实验)为了确定离子组成,小红同学取无色滤液于试管中向其中加入少量碳酸钠溶液,只观察到溶液中产生气泡的现象,于是他得出结论:无色滤液中的离子组成一定为Cl-、H+或Cl-、H+、SO42-中的一种。
请你对他的说法进行评价:________。
经过分析小红的实验,小桥取小红实验后的废液同时还选用碳酸钠溶液,最终确定出了离子的组成为上述四种猜想中的一种,他的实验方法是:________。
(4)(反思与归纳)归纳一:分析上述区分物质方法时,我们可以归纳出如果溶液中的两种物质都含有相同的离子则可以加入合理的试剂只需验证________,就可以将两种物质做出区分:所以鉴别不同物质的原则是依据物质性质的差异设计实验,且实验中还要________;
归纳二:验证溶液中离子成分时,若加入的试剂与两种离子都能反应时则需要考虑________,此时药品的用量也可能会对实验结论的判断产生影响。
【答案】2FeCl3+3Ba(OH)2=2Fe(OH)3↓+3BaCl2 漏斗、烧杯、玻璃棒、滤纸 不正确,向滤液中加入少量碳酸钠溶液,只观察到溶液中产生气泡,只能说明溶液中含有氢离子,但也无法确定钡离子是否存在,若溶液中的离子组成为Cl-、H+、Ba2+时,加入少量碳酸钠溶液,碳酸钠先与氢离子反应而被耗尽,没有与钡离子反应也会产生上述现象,所以他的结论不正确 继续加入碳酸钠溶液至过量,(观察到溶液中产生气泡,)而后溶液中出现白色沉淀,确定离子组成为Cl-、H+、Ba2+ 两物质中的不同离子 产生不同的明显的实验现象(或分别产生明显唯一的实验现象) 反应的先后顺序
【解析】
氢氧化钡与二氧化碳反应生成碳酸钡沉淀和水,氯化铁与氢氧化钡反应生成氢氧化铁沉淀和氯化钡,氯化钡与硫酸反应生成硫酸钡沉淀和盐酸。
(1)若在C组的①试管中观察到溶液中产生白色沉淀这一明显实验现象,证明①是氢氧化钡溶液,氢氧化钡与二氧化碳反应生成碳酸钡沉淀和水,则B组中①试管内发生反应为氯化铁与氢氧化钡反应生成氢氧化铁沉淀和氯化钡,反应的化学方程式为2FeCl3+3Ba(OH)2=2Fe(OH)3↓+3BaCl2。
(2)在过滤操作中需要的用品除了带铁圈的铁架台以外还需要漏斗、烧杯、玻璃棒、滤纸,然后对所得滤液中离子的组成进行探究。
(3)[设计实验]碳酸根离子和氢离子生成二氧化碳和水,氯化钡与硫酸反应生成硫酸钡沉淀和盐酸,故他的说法不正确,向滤液中加入少量碳酸钠溶液,只观察到溶液中产生气泡,只能说明溶液中含有氢离子,但也无法确定钡离子是否存在,氯化钡与硫酸反应,生成硫酸钡沉淀和盐酸。若溶液中的离子组成为Cl-、H+、Ba2+时,加入少量碳酸钠溶液,碳酸钠先与氢离子反应而被耗尽,没有与钡离子反应也会产生上述现象,故他的结论不正确。
碳酸根离子与钡离子生成碳酸钡沉淀,故实验方法是继续加入碳酸钠溶液至过量,(观察到溶液中产生气泡,)而后溶液中出现白色沉淀,碳酸根离子与钡离子结合生成碳酸钡沉淀,确定离子组成为Cl-、H+、Ba2+。
(4)归纳一:区分物质方法时,如果溶液中的两种物质都含有相同的离子则可以加入合理的试剂只需验证两物质中的不同离子,就可以将两种物质做出区分:鉴别不同物质的原则是依据物质性质的差异设计实验,且实验中还要产生不同的明显的实验现象(或分别产生明显唯一的实验现象)。
归纳二:验证溶液中离子成分时,若加入的试剂与两种离子都能反应时则需要考虑反应的先后顺序,此时药品的用量也可能会对实验结论的判断产生影响。