题目内容
某纯净物M微热就能分解生成NH3、H2O和CO2,由此得出的结论是M由 元素组成,2.6克可燃物在氧气中燃烧,生成4.4克二氧化碳和3.6克水,则该可燃物中含有 元素.
考点:质量守恒定律及其应用
专题:化学用语和质量守恒定律
分析:化学反应前后,元素的种类不变,原子的种类、总个数不变.
解答:解:某纯净物M微热就能分解生成NH3、H2O和CO2,由此说明M由氮元素、氢元素、氧元素和碳元素组成;
4.4g二氧化碳中碳元素的质量为:4.4g×
×100%=1.2g;
3.6g水中氢元素的质量为:3.6g×
×100%=0.4g;
根据质量守恒定律可知,二氧化碳中的碳元素和水中的氢元素来自于该可燃物,则该可燃物中含有氧元素的质量为:2.6g-1.2g-0.4g=1.0g,
即该可燃物中含有碳元素、氢元素和氧元素.
故填:N、H、O、C;C、H、O.
4.4g二氧化碳中碳元素的质量为:4.4g×
| 12 |
| 44 |
3.6g水中氢元素的质量为:3.6g×
| 2 |
| 18 |
根据质量守恒定律可知,二氧化碳中的碳元素和水中的氢元素来自于该可燃物,则该可燃物中含有氧元素的质量为:2.6g-1.2g-0.4g=1.0g,
即该可燃物中含有碳元素、氢元素和氧元素.
故填:N、H、O、C;C、H、O.
点评:化学反应遵循质量守恒定律,即化学反应前后,元素的种类不变,原子的种类、总个数不变,这是书写化学方程式、判断物质的化学式、判断化学计量数、进行相关方面计算的基础.

练习册系列答案
 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案
相关题目
原子中质量最小的是( )
| A、电子 | B、质子 | C、原子核 | D、中子 |
下列对物质世界的认识中不正确的是( )
| A、为提高粮食产量,应大量使用化肥和农药 |
| B、化学为人类研究开发了大量新型材料 |
| C、废旧金属的回收利用是保护金属资源的有效途径 |
| D、海洋中蕴藏着丰富的资源 |
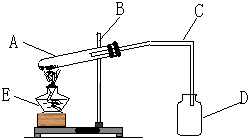
 程伟同学将浑浊的湖水样品倒入烧杯中,先加入明矾粉未搅拌溶解,静置一会儿后,采用如图所示装置进行过滤,请问:
程伟同学将浑浊的湖水样品倒入烧杯中,先加入明矾粉未搅拌溶解,静置一会儿后,采用如图所示装置进行过滤,请问: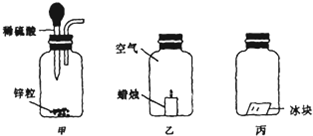
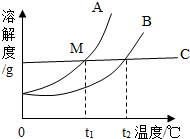 根据图中A、B、C的溶解度曲线回答:
根据图中A、B、C的溶解度曲线回答: