题目内容
氧化铜有多种用途,如作玻璃着色剂、油类脱硫剂等.为获得纯净的氧化铜以探究其性质,某同学用工业硫酸铜固体(含硫酸亚铁等杂质)进行如下实验:(1)制备氧化铜:工业CuSO4

 CuSO4溶液
CuSO4溶液 CuSO4?5H2O→…→CuO
CuSO4?5H2O→…→CuO①步骤Ⅰ的目的是除去不溶性杂质.步骤Ⅰ的操作是:______.
②步骤Ⅱ的目的是除铁.
③步骤Ⅲ的目的是得到CuSO4?5H2O晶体,操作是:______、过滤、水浴加热烘干(水浴加热的特点是受热均匀,温度易于控制在100℃以下)
④制备氧化铜(略)
(2)探究氧化铜的性质
①取A、B两支试管,往A中加入适量的CuO粉末,再分别向A和B加入等体积3%H2O2溶液,只观察到A中有大量气泡,结论是:______
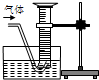
②为探究试管A中的反应速率(单位以mL/s表示),用如图所示装置收集气体并测定其体积,实验中还必需用到的仪器是:______.
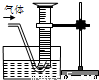
【答案】分析:(1)①根据除去混合物中不溶性的杂质的分离方法分析;
③根据题意,将CuSO4溶液加热蒸发至饱和状态即可;
(2)通过反应现象比较,可以看出:CuO可加快过氧化氢分解的反应速率,充当了催化剂的角色;
②根据探究试管A中的反应速率需要计时分析;
解答:解:(1)①除去混合物中不溶性的杂质,可以先溶解、在过滤,在溶解的过程中必须用玻璃棒搅拌,故答案为:加适量的水溶解、搅拌、过滤;
③将CuSO4溶液加热蒸发至有晶体析出现时,即饱和状态,停止加热,然后用水浴加热烘干就可得到CuSO4?5H2O晶体,故答案为:将CuSO4溶液加热蒸发至有晶体析出现时,停止加热;
(2)通过反应现象比较,可以看出:CuO可加快过氧化氢分解的反应速率,是该反应的催化剂,故答案为:CuO可加快过氧化氢分解的反应速率,是过氧化氢分解反应的催化剂;
②根据题意需用用时间来探究试管A中的反应速率,故答案为:计时器
点评:本题是一道实验探究题,能较好的考查学生分析和解决问题的能力,考查了常见物质分离的方法,解答时要依据题干提供信息,结合相关知识细心分析解答.
③根据题意,将CuSO4溶液加热蒸发至饱和状态即可;
(2)通过反应现象比较,可以看出:CuO可加快过氧化氢分解的反应速率,充当了催化剂的角色;
②根据探究试管A中的反应速率需要计时分析;
解答:解:(1)①除去混合物中不溶性的杂质,可以先溶解、在过滤,在溶解的过程中必须用玻璃棒搅拌,故答案为:加适量的水溶解、搅拌、过滤;
③将CuSO4溶液加热蒸发至有晶体析出现时,即饱和状态,停止加热,然后用水浴加热烘干就可得到CuSO4?5H2O晶体,故答案为:将CuSO4溶液加热蒸发至有晶体析出现时,停止加热;
(2)通过反应现象比较,可以看出:CuO可加快过氧化氢分解的反应速率,是该反应的催化剂,故答案为:CuO可加快过氧化氢分解的反应速率,是过氧化氢分解反应的催化剂;
②根据题意需用用时间来探究试管A中的反应速率,故答案为:计时器
点评:本题是一道实验探究题,能较好的考查学生分析和解决问题的能力,考查了常见物质分离的方法,解答时要依据题干提供信息,结合相关知识细心分析解答.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目

 氧化铜有多种用途,如作玻璃着色剂、油类脱硫剂等.为获得纯净的氧化铜以探究其性质,某同学用工业硫酸铜固体(含硫酸亚铁等杂质)进行如下实验:
氧化铜有多种用途,如作玻璃着色剂、油类脱硫剂等.为获得纯净的氧化铜以探究其性质,某同学用工业硫酸铜固体(含硫酸亚铁等杂质)进行如下实验: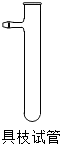

 CuSO4溶液
CuSO4溶液 CuSO4·5H2O→……→CuO
CuSO4·5H2O→……→CuO 