题目内容
【题目】某钙片标签的部分内容如右图(钙片中只有碳酸钙含有钙元素),则下列说法错误的是

A. 钙元素是人体所需的微量元素
B. 每片钙片中含有钙元素的质量为0.30g
C. 碳酸钙中钙、碳、氧三种元素质量比为10:3:12
D. 药品中的碳酸钙会和胃里的盐酸发生复分解反应
【答案】A
【解析】A.钙元素是人体所需的常量元素;
B.根据碳酸钙中钙元素的质量分数计算解答;
C. 根据碳酸钙中各元素的质量比解答;
D.根据胃酸的主要成分是盐酸解答。
解:A.钙元素是人体所需的常量元素。故说法错误;
B. 每片钙片中含有钙元素的质量为0.75g×40%=0.30g。正确。
C. 碳酸钙中钙、碳、氧三种元素质量比为40:12:(16×3)=10:3:12。正确;
D. 药品中的碳酸钙会和胃里的盐酸发生复分解反应。说法正确。

 英才计划期末调研系列答案
英才计划期末调研系列答案 精英口算卡系列答案
精英口算卡系列答案【题目】化学兴趣小组的同学发现实验室有一瓶失去标签的黑色粉末,可能是炭粉、铁粉、二氧化锰或氧化铜中的一种,为了探究其成分,同学们设计了如下实验方案:
(1)实验:
步骤 | 操作 | 现象 | 结论 |
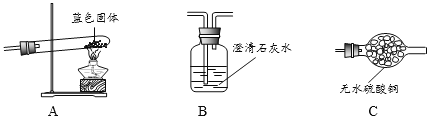
① | 取少量粉末放在燃烧匙中,放在酒精灯火焰上灼烧。罩上内壁附有石灰水的烧杯。 | 若烧杯内壁的石灰水 ____________________ | 则粉末为炭粉 |
② | 取少量粉末于试管中,滴入足量稀硫酸。 | 将燃着的木条放在试管口,若有尖锐的爆鸣声。 | a.则粉末为____。 |
b.若黑色固体消失,_______ | 则粉末为氧化铜。 | ||
③ | 取少量固体于试管中,滴入5%的过氧化氢溶液,将带火星的木条伸入试管中。 | 若产生大量气泡,且 ___________________ | 则粉末为______。 |
(2)表达:
步骤①的化学方程式_____________________________、________________________。
步骤③的化学方程式_______________________________________________________。
(3)拓展:老师指出,步骤①不严密,你认为原因是:________________________。